


| 选项 | 物质 | 杂质 | 实验方案 |
| A | H2 | HCl | 通入足量NaOH溶液,干燥 |
| B | CuO | Cu | 加入适量稀盐酸,过滤 |
| C | FeSO4溶液 | CuSO4 | 加入过量的铁粉,过滤 |
| D | NaCl溶液 | Na2SO4 | 加入过量的BaCl2溶液,过滤 |
①一种可燃性气体;
②一种易挥发的酸;
③一种难溶性的碱;
④一种金属氧化物;
⑤一种用作调味品的盐。


①纤维素属于选填(“有机物”“无机物”“氧化物”之一)。
②纤维素由种元素组成。
③纤维素分子中,H、O原子的个数比为(最简整数比)。
④纤推素中,C、H元素的质量比为(最简整数比)。
⑤纤维素中,所含元素的质量分数最小的为(填元素符号)。
①青铜属于(选填“复合材料”“有机高分子材料”“金属材料”“无机非金属材料”之一)。
②我们的祖先很早就掌握了炼铜的工艺,他们将孔雀石(主要成分是Cu2(OH)2CO3)和木炭一起加热就可得到红色的铜。首先孔雀受热分解可得到CuO,再用木炭做还原剂加热,把氧化铜中的铜还原出来,生成一种能使澄清的石灰水变浑浊的气体。请写出木炭还原氧化铜的反应方程式,在此过程中C元素的化合价在反应前后的变化情况是(选填“升高”“降低”“不变”之一)。

①t1℃时,NaCl的溶解度Na2CO3的溶解度(选填“大于”“等于”“小于”之一)。
②t1℃时,100g水中加入20g Na2CO3固体,经充分溶解,所得溶液中溶质与溶液的质量之比为(填最简整数比)。
③t2℃时,将相同质量的碳酸钠饱和溶液和氯化钠饱和溶液降温至t1℃,析出晶体的质量碳酸钠氯化钠(选填“大于”“等于”“小于”“无法判断”之一)。

①制取并收集干燥的氧气所选仪器的连接顺序为(填写仪器序号字母),MnO2在反应前后的质量(选填“增大”“减小”“不变”之一)。
②上述制取氧气的化学反应方程式为。
①仪器C处大玻璃管内出现的反应现象为。
②装置D的作用是,装置B的作用是。
③通过测量反应前后C处大玻璃管的质量变化,来计算氧化铁的纯度。若其他操作正确,反应结束熄灭酒精灯后,维续通入一氧化碳气体,直至大玻璃管冷却,则这样计算出的氧化铁样品纯度与实际值比较将(填“一定偏大”“一定片少”“基本一致”之一)。
④在这个实验装置中,除了可以利用反应前后C处大玻璃管的质量数据变化来计算氧化铁样品的纯度外,还可以通过测量装置B质量的变化来计算氧化铁样品的纯度,若装置B增重0.66g,则样品中Fe2O3的质量为g。
⑤小强同学设计的这套实验装置是否存在不足之处,若有请写出你的具体改进建议。
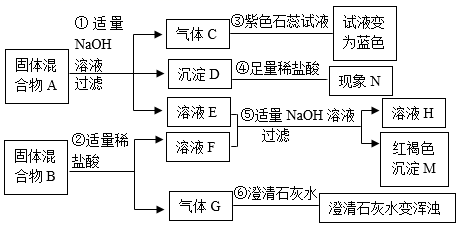
试根据实验过程和图示提供的信息进行分析推理,填写以下空白:

①根据实验目的,小明同学应该测量的数据是(选填“只有反应前”“只有反应后”“反应前后”之一)整个反应装置(包括锥形瓶、气球和药品)的质量。
②实验步骤如下:
Ⅰ、按如图方式放好仪器,使天平平衡,记录称量数据。
Ⅱ、将碳酸钙粉末全部倒入锥形瓶中,观察到的现象为(写出一条即可)。
Ⅲ、当反应结束时,气球已经完全鼓起,小明发现天平的指针略向右偏,小明又重新实验,发现指针仍略向右偏。
他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符?你认为出现该实验现象的合理解释最应该是下列各项中的(填序号)
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵质量守恒定律

①当滴入稀盐酸50g时,烧杯中溶液里一定大量存在的金属阳离子是(请写出离子符号)。
②样品中Na2CO3的质量是多少?(写出计算过程,计算结果精确至0.1g)