| 选项 | 实验操作和现象 | 结论 |
| A | 浓硝酸久置于空气,颜色略显黄色 | 浓硝酸具有不稳定性 |
| B | 铜丝伸入到稀硝酸中,溶液变蓝,有气泡产生 | Cu与稀硝酸发生置换反应 |
| C | 向蔗糖中滴入浓硫酸,固体变黑膨胀 | 浓硫酸具有吸水性 |
| D | SO2通入含有酚酞的氢氧化钠溶液,溶液褪色 | SO2具有漂白性 |

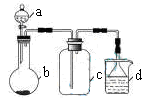
| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸(70%) | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |

 B . 比较
B . 比较  C . 除去
C . 除去  D . 验证氨气易溶于水
D . 验证氨气易溶于水 


a、可通过雷电作用将b转化为c,这是一种固氮方式
b、可通过加氧化剂将e转化为f
c、a→c→d→f这几个反应中,均发生了N元素被氧化的反应
d、g只具有氧化性,还可能与碱发生反应
e、可通过加Cu、C等还原剂,将f转化为d
f、h可与f反应生成i
任务Ⅰ.从以下试剂中选择合适的试剂实现 的转化。
试剂:①浓H2SO4 ②稀H2SO4 ③酸性 溶液 ④
溶液 ⑤Cu ⑥品红溶液
任务Ⅱ.实现硫元素在 、
、
价之间的转化。
查阅资料: 价硫元素在酸性条件下不稳定,自身易发生氧化还原反应。

①氨气的发生装置可以选择上图中的,反应的化学方程式为。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→(按气流方向,用小写字母表示)。
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1 , 推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中 | ②反应的化学方程式
|
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
| 打开K2 | ③ | ④ |
|
化学键 |
C-H |
C=O |
H-H |
C=O(CO) |
|
键能/KJ.mol-1 |
413 |
745 |
436 |
1075 |
ΔH=