B .
B .  C .
C .  D .
D . 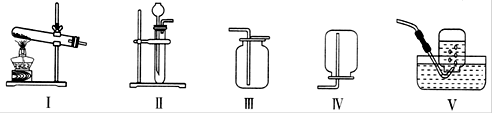

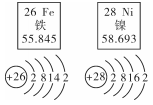
 衬衫1的“2Fe"表示:两个铁离子
B .
衬衫1的“2Fe"表示:两个铁离子
B .  创意钟表里全是非金属元素
C .
创意钟表里全是非金属元素
C .  衬衫2表示的化学方程式:Mg+ZnSO4= MgSO4+Zn
D .
衬衫2表示的化学方程式:Mg+ZnSO4= MgSO4+Zn
D .  图4对应的微粒符号:Na+
图4对应的微粒符号:Na+

| 选项 | 实验目的 | 实验方案 |
| A | 鉴别 CH4和 H2 | 点燃后分别在火焰上方罩一个冷而干燥的烧杯 |
| B | 鉴别羊毛和涤纶 | 分别取样,灼烧,闻气味 |
| C | 除去 KNO3溶液中的 KCl | 加入过量 AgNO3溶液,过滤 |
| D | 除去铁粉中的少量铜粉 | 加入足量稀盐酸,充分反应后过滤、洗涤、干燥 |
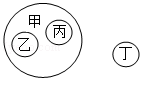
| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | 化合物 | 盐酸 | MnO2 | 铁粉 |
| B | 合成材料 | 合金 | 合成纤维 | 合成橡胶 |
| C | 化学变化 | 置换反应 | 化合反应 | 复分解反应 |
| D | 放热反应 | 硫在空气中燃烧 | NaOH溶液与稀H2SO4反应 | 高温分解石灰石 |
野炊食谱如下:主食:馒头;配菜:红烧肉、豆腐汤、牛肉干。从营养角度来看,你认为食谱中还应添加下列食品中的(填序号)。
A 黄瓜 B 面条 C 炒鸡蛋 D 糖醋鱼
①深冷空气制氮。利用空气各成分的沸点不同,使液态空气中的氧气和氮气分离,液态氧的沸点是-183℃,液态氮的沸点是-196℃,则分离出来某气体后,剩下的主要是。
②变压吸附制氮。利用碳分子筛对氮气进行吸附,可见碳分子筛与一样具有疏松多孔的结构,可用于水的净化。
③膜分离制氮。利用中空纤维膜分离空气制取氮气。中空纤维膜还常用于自来水、地下水除菌除浊净化,使水中的微粒、细菌等不能通过滤膜而被去除。
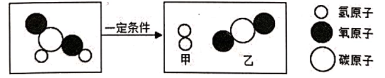
12C、13C、14C分别表示碳元素的三种原子,可简写成12C、13C、14C。请据图回答:
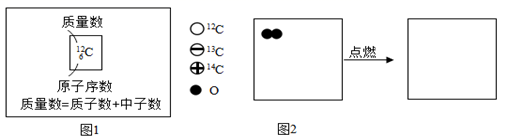
①12C、13C、14C三种原子中,数目不等(填“质子”或“中子”或“电子”)。
②12C与O2反应生成的一氧化碳可表示为12CO。写出13CO在O2中燃烧的化学方程式,在图2所示的小方框中,把13CO与O2反应的反应物和生成物微观粒子补画齐全。(画在答题卡上)
(1)请以表2中序号Ⅰ为示例,填写序号Ⅱ、Ⅲ中的空格:
|
项目 序号 |
举例 |
物质类别间的相互反应 |
物质类别间的相互转化 |
|
Ⅰ |
CaCl2+Na2CO3=CaCO3↓+2NaCl |
盐1﹣盐2 |
盐→新盐 |
|
Ⅱ |
写出硫酸与氯化钡反应的化学方程式 |
酸﹣盐 |
酸→ |
|
Ⅲ |
写出氢氧化钠转变成另一种碱的 |
碱﹣ |
碱→新碱 |
(2)室温下,氯化镁与下列物质的变化关系,正确的是 (填标号).
A.MgCl2﹣AgNO3
B.KNO3﹣MgCl2
C.MgCl2﹣HCl
D.Mg(OH)2﹣MgCl2 .
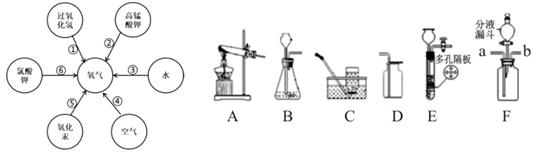
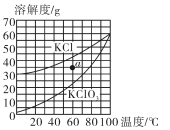
途径⑥需要添加 Mn2 作催化剂,若反应结束后回收 MnO2 固体,需进行的操作是溶解、.、洗涤、烘干。
①从 b 端通氮气;②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中;③从 a 端通二氧
化碳;④从分液漏斗中滴加适量水。
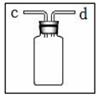
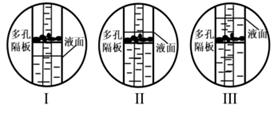
[提出假设]
假设1:生成CO2造成的。
假设2:生成CaCl2造成的。
假设3:剩余稀盐酸造成的。
[设计实验]
|
实验编号 |
实验操作 |
实验现象 |
|
① |
取氯化钙溶于水,测定溶液的pH |
测得pH=7 |
|
② |
将CO2通入蒸馏水中至饱和,测定溶渡的pH |
测得pH>5 |
[设计实验]
剩余液pH=2的原因是。
①由此得出的结论是:写出反应的化学方程式:。
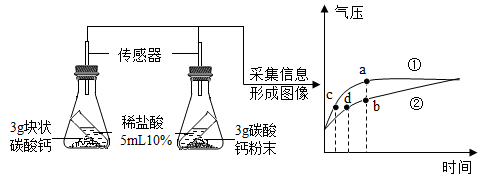
②比较稀盐酸加入前后的实验现象,解释 “又有大量气泡产生”的原因:。
假如用100 g 14. 6%的稀盐酸和足量的石灰石反应,观察不到气泡产生时,停止收集气体,收集到的CO2质量(填“> ”“<”或“=”)8.8g。

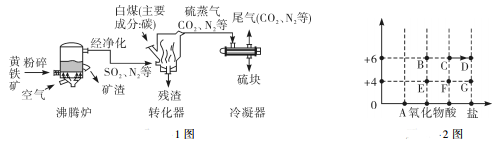
已知:沸腾炉中的主要反应为4FeS2+11O2 2Fe2O3+8SO2。