 )用于改善肌强直和运动迟缓效果明显,下列有关该物质的说法错误的是( )
)用于改善肌强直和运动迟缓效果明显,下列有关该物质的说法错误的是( )
| A | B | C | D |
| | | | |
| 分离四氯化碳与水 | 除去食盐水中的泥沙 | 制备乙酸乙酯 | 分离苯和硝基苯 |

| 选项 | 实验目的 | 实验操作 |
| A | 除去 | 将混合气体通过饱和 |
| B | 配制 | 将 |
| C | 比较 | 同温下,用 |
| D | 除去 | 将固体溶于水配成溶液,蒸发浓缩、冷却结晶 |
①每次取废水样品amL,用 溶液进行处理,将
转化为毒性较低的
,同时
转化为
,平均每次消耗了vmL。废水中
为。(用含a、b、v的式子表示)。
②室温下,将上述溶液再调节至 ,使
转化成
而沉降,分离出污泥,检测到废水中
浓度约为
,室温下
。
已知:① (紫色)
② 遇
无明显现象
③ 能显著减慢
的紫色褪去
|
实验编号 |
I |
II |
|
实验操作 |
|
|
|
实验现象 |
溶液呈紫色,静置后紫色迅速褪去,久置后出现淡黄色浑浊 |
溶液呈紫色,静置后紫色较快褪去,久置后未出现淡黄色浑浊 |
已知:2Li2O(s)+SiO2(s)=Li4SiO4(s) ΔH1=akJ⋅mol-1
Li2CO3(s)+SiO2(s)=Li2SiO3(s)+CO2(g) ΔH2=bkJ⋅mol-1
Li2SiO3(s)=Li2O(s)+SiO2(s) ΔH3=ckJ⋅mol-1
则2Li2CO3(s)+SiO2(s)=Li4SiO4(s)+2CO2(g) ΔH=kJ⋅mol−1(用含a、b、c的式子表示)。
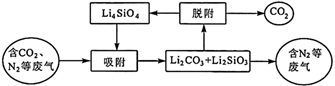
“吸附”过程中主要反应的化学方程式为。
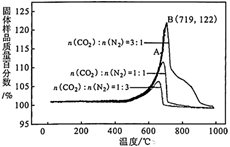
①该反应为反应(填“吸热”或“放热”)。
②A点的v正v逆(填“>”、“<”或“=”),理由是。
③不同CO2的体积分数对于吸附速率的影响是。
④保持B点的温度不变,若所用刚性容器体积为原来的一半,则平衡时理论上c(CO2)较原平衡(填“增大”、“减小”或“不变”)。
⑤B点CO2的吸收率为(保留3位有效数字)。
I.四苯基金属锌卟啉配合物具有促进细胞组织呼吸、改善蛋白质和糖代谢等作用,其合成过程如下(ph-为苯基):


钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的空隙中,若Ca2+与O2-的最短距离为anm,设NA为阿伏加德罗常数的值,则晶体的密度为g∙cm-3(列出计算表达式)。
①苯环上有两个对位取代基
②能与FeCl3溶液发生显色反应