 B .
B .  C .
C .  D .
D . 

| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 1 | 10 | 27 | 4 |
| 反应后质量/g | 1 | a | 0 | 23 |
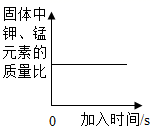 B . 氯化铁和盐酸的混合溶液中加入氢氧化钠溶液至过量
B . 氯化铁和盐酸的混合溶液中加入氢氧化钠溶液至过量 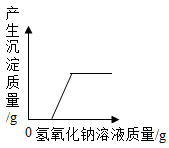 C . 一定质量的AgNO3和 Cu(NO3)2的混合溶液中加入足量Fe粉
C . 一定质量的AgNO3和 Cu(NO3)2的混合溶液中加入足量Fe粉 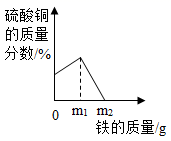 D . 稀盐酸与氢氧化钠溶液反应过程中pH变化曲线,X表示氢氧化钠溶液
D . 稀盐酸与氢氧化钠溶液反应过程中pH变化曲线,X表示氢氧化钠溶液 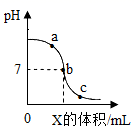
A.小苏打 B.二氧化硫 C.金刚石 D.生石灰
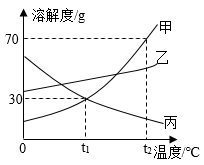
(查阅资料)
(工艺流程)为从某锈蚀的铜样品中回收铜并制得硫酸锌,取该铜样品(除含有铜、锌和铜绿外,不含其它物质),进行如下操作:

请回答下列问题:
①气体a中含有H2和(填化学式),溶液A的颜色为色。
②操作Ⅰ的名称是,该操作中玻璃棒的作用是。
③写出②中发生反应的化学方程式(写一个即可),该反应属于基本反应类型中的反应。

已知:燃烧器中发生的主要反应为
①热气中一定含有的物质有(写一种即可)。
②通过上述反应,你对燃烧条件的新认识是。
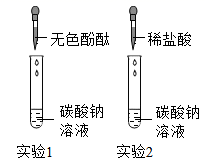
(实验2)往另一支盛有碳酸钠溶液的试管中滴加稀盐酸,观察到的现象是。同学们对实验2反应后的废液中溶质成分进行探究。
(作出猜想)猜想一:废液中的溶质可能是NaCl、HCl
猜想二:废液中的溶质可能是NaCl、Na2CO3
猜想三:废液中的溶质可能是。
方案一:
|
实验操作与现象 |
反应方程式 |
实验结论 |
|
小芳取少量废液于试管中,滴加澄清石灰水,有白色沉淀产生 |
|
猜想二正确 |
(进行讨论)同学们一致认为小明的实验结论不正确,理由是。

①产生CO2的质量为克。
②所用稀盐酸中溶质的质量分数是多少?(写出具体的解题过程,下同)
③滴入稀盐酸至恰好完全反应时,所得溶液中溶质的质量分数是多少?