 B . 测定空气中氧气的含量
B . 测定空气中氧气的含量  C . 收集气体
C . 收集气体  D . 铁丝燃烧
D . 铁丝燃烧 
 分离H2O2和MnO2制O2后的固液混合物
B .
分离H2O2和MnO2制O2后的固液混合物
B . 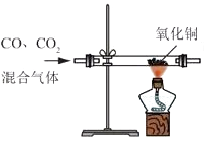 除去CO中的CO2气体
C .
除去CO中的CO2气体
C .  区分NaCl、NH4NO3、NaOH三种固体
D .
区分NaCl、NH4NO3、NaOH三种固体
D . 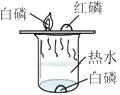 探究可燃物燃烧的条件
探究可燃物燃烧的条件

| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | H2(HCl) | 依次通过饱和碳酸氢钠溶液和浓硫酸 |
| B | CaO(CaCO3) | 高温煅烧 |
| C | NaOH溶液(Na2CO3) | 加足量稀盐酸 |
| D | NaCl溶液(MgCl2) | 加适量氢氧化钾溶液,充分反应后过滤 |

①干馏 ②分馏 ③氧化 ④乳化 ⑤挥发 ⑥催化


H2SO4中,硫元素的化合价为。
①用量筒量取浓硫酸时仰视刻度
②稀释后,用水冲洗搅拌的玻璃棒,并将洗涤液并入稀释后的硫酸
③将配置好的稀硫酸转移至细口瓶时,有少许液体洒出
向氧化铜粉末中加入一定量的稀硫酸,待固体完全消失后,再缓缓滴加氢氧化钠溶液,获得沉淀质量随氢氧化钠质量的变化关系如图所示。

a点所得溶液的pH7(选填>、<=)。


①装有石灰石的塑料瓶底部用剪刀戳了一些小孔,则此发生装置的优点是。
②打开K1、K2、K3 , 关闭K4 , 可以看到(选填“高”或“低”)的蜡烛先熄灭。
③打开K1、K4 , 关闭K2、K3 , 一段时间后,大号塑料瓶中出现的现象是,小号塑料瓶中发生反应的化学方程式为。
④该大号塑料瓶的容积为2.2L,若需将其充满二氧化碳(密度为2g/L),至少需要含碳酸钙80%的石灰石多少g?(根据化学方程式计算,写出计算过程)



①实验进行时试管内发生的化学反应是(写出化学方程式)。
②小华认为选择活性炭和氧化铁反应更适合,他的理由是。
③通过对图两幅图像的分析,90秒至300秒之间一氧化碳含量变化趋势明显不同的主要原因可能是。

资料卡:①SiO2既不溶于水,也不溶于常见的酸。
②“沉淀”时,通入CO2是为了调节提纯液的pH。

资料卡:①碱石灰是氢氧化钠固体和生石灰的混合物。
②无水硫酸铜是白色固体,遇水变蓝。
(猜想假设)1.H2O; 2.CO2; 3.NH3
其中猜想3明显不合理,理由是。
(实验结论)通过上述实验现象得知,碱式碳酸锌受热分解后有水和二氧化碳生成。

重新组装仪器,虚线框A处是换装了浓硫酸的装置①,浓硫酸的作用是;在虚线框B处是连续的2个装置②。