
| A | B | C | D |
| | | | |
| 探究燃烧的条件 | 除去CO中混有的CO2 | 检查装置的气密性 | 检验氢氧化钠固体溶于水时放热 |
 向一定量氢氧化钠和氯化钡的混合溶液中,逐滴滴加稀硫酸
B .
向一定量氢氧化钠和氯化钡的混合溶液中,逐滴滴加稀硫酸
B .  向一定量灼热的氧化铜中通入一氧化碳气体
C .
向一定量灼热的氧化铜中通入一氧化碳气体
C .  向一定量的饱和硫酸铜溶液中不断加入无水硫酸铜
D .
向一定量的饱和硫酸铜溶液中不断加入无水硫酸铜
D .  向一定量的稀硫酸中加入足量的铁片
向一定量的稀硫酸中加入足量的铁片

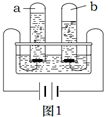
①图1是水通电分解的示意图,该反应的化学方程式为,b管中产生的气体是。
②家用净水器中通常加入活性炭,其作用是。
③图2是甲、乙、丙三种固体物质的溶解度曲线。请根据图回答下列问题:
Ⅰ.t3℃时,甲、乙、丙三种物质溶解度大小关系是。
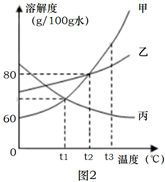
Ⅱ.若甲中混有少量的乙,提纯甲物质可采取的方法是。
Ⅲ.在t2℃时,配制90g甲物质的饱和溶液,需要甲物质的质量是g。
Ⅳ.t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温到t1℃,下列叙述正确的是(填字母序号)。
A.溶质质量分数的大小关系是:乙>甲>丙
B.溶剂质量的大小关系是:丙>乙>甲
C.溶液质量的大小关系是:丙>乙>甲
D.析出固体质量的大小关系是:甲>乙>丙

①写出仪器a的名称。
②通常实验室制取CO2的化学方程式是。用B装置制取CO2时,反应未停止前关闭止水夹,除了有气泡产生外,还可观察到的现象是。选择(填装置编号)装置作为制取CO2的发生装置具有随时控制反应发生和停止的优点。若用E装置收集CO2 , 气体应从处通入(填“m”或“n”)。
③实验室用过氧化氢溶液和二氧化锰制取氧气,若产生0.2mol氧气,则参加反应的过氧化氢的质量为g。(根据化学方程式计算)。

①如图1所示,该实验中观察到的现象是可证明氢氧化钠溶液和稀盐酸发生反应,反应的化学方程式为。
取上述实验后的溶液于试管中,为验证氢氧化钠溶液和稀盐酸是否恰好完全反应,理论上可选择的试剂是。
A.铜片B.碳酸钠溶液C.硝酸银溶液
②为探究中和反应过程中热量的变化情况,某实验小组进行了以下三个对比实验,并用温度传感器测定实验过程中的温度变化情况,得到了如图2所示的三根曲线:
实验1:50mL一定浓度的盐酸与50mL一定浓度的氢氧化钠溶液混合(曲线a);
实验2:50mL一定浓度的盐酸与50mL蒸馏水混合(曲线b);
实验3:50mL一定浓度的氢氧化钠溶液与50mL蒸馏水混合(曲线c)。

Ⅰ.对比三根曲线,根据曲线a可以得到的结论是。
Ⅱ.结合实验目的,请分析实验小组增加实验2、实验3的理由。
某氯化钠样品中混有少量泥沙、氯化钙及硫酸钠,为得到纯净的氯化钠,实验小组设计了如下的流程:

①加足量水的目的是。操作①的名称是。
②实验过程中,实验小组选择两种不同的盐溶液进行了操作②和操作③,请根据题意在虚线方框内写出操作②和操作③的具体做法。
③实验小组同学发现最终得到的氯化钠质量大于样品中所含的氯化钠质量,原因是(用化学方程式表示,写出一个即可):。