

| 选项 | 实验操作和现象 | 结论 |
| A | 乙醇钠的水溶液呈强碱性 | |
| B | 将某溶液滴在 | 原溶液中一定含有 |
| C | 向 | 氧化性: |
| D | 向盛有 | |

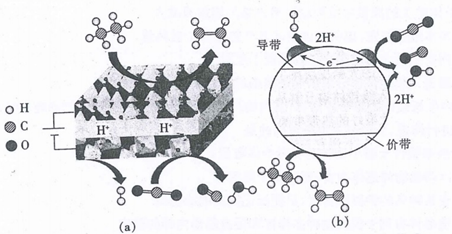
已知:①“净化除杂”时采用真空蒸馏的方法提纯硒(沸点为685℃);
②焙烧后,Cu、Ag均以硫酸盐形式存在, ;
③“浸出液”中溶质的饱和浓度不小于0.01 。
下列说法错误的是( )

|
与F的相对位置 |
邻 |
间 |
对 |
其他 |
|
含量/% |
38.8 |
3.66 |
57.25 |
0.29 |
请找出规律:。
Ⅰ.苯环上只有三个取代基且处于邻位,且—SH、—F直接与苯环相连;
Ⅱ.能发生银镜反应;
Ⅲ.能与NaHCO3溶液反应。
Ⅰ.CO(g)+2H2(g) CH3OH(g)△H1=-90.8kJ·mol-1
Ⅱ.2CH3OH(g) CH3OCH3(g)+H2O(g)△H2=-23.5kJ·mol-1
A.再通入一定量的CO B.降低温度
C.及时移走CH3OCH3(g) D.通入氮气

达到平衡后,增大压强,反应Ⅰ的平衡(填“向正反应方向”、“向逆反应方向”或“不”,下同)移动,反应Ⅱ的平衡移动,故工业上选择(填“高压”或“低压”)制备二甲醚。工业生产中不选择350℃的原因是。
