

 Cl-的物质中含有不对称原子P,该物质可能有旋光性
C . SiCl4、PCl3、SCl2中键角最大的是PCl3
D . 实验测定分子的极性大小可以区别顺-1,2-二氯乙烯和反-1,2-二氯乙烯
Cl-的物质中含有不对称原子P,该物质可能有旋光性
C . SiCl4、PCl3、SCl2中键角最大的是PCl3
D . 实验测定分子的极性大小可以区别顺-1,2-二氯乙烯和反-1,2-二氯乙烯




 已知:钛铁矿经盐酸浸取后钛主要以
已知:钛铁矿经盐酸浸取后钛主要以 形式存在,
、
。下列说法错误的是( )

|
选项 |
实验操作和现象 |
结论 |
|
A |
向纤维素中加入适量硫酸溶液,微热一段时间后,滴加新制的氢氧化铜悬浊液,加热煮沸,未发现砖红色沉淀生成 |
纤维素没有水解或者已经水解但水解后的产物中没有葡萄糖 |
|
B |
1-溴丙烷与NaOH的乙醇溶液共热,有气体生成,该气体可使酸性高锰酸钾溶液褪色 |
该气体是丙烯 |
|
C |
粗盐提纯时,将2mol·L-1NaOH、饱和BaCl2和0.5mol·L-1Na2CO3溶液依次加入后,一次过滤,滤液用HCl调至pH<3,取少许该溶液滴加饱和BaCl2溶液,发现有明显的白色沉淀生成 |
说明“一次过滤”后没有完全除尽 |
|
D |
向苯酚钠溶液中通入CO2 , 溶液变浑浊 |
碳酸溶液的pH比苯酚小 |

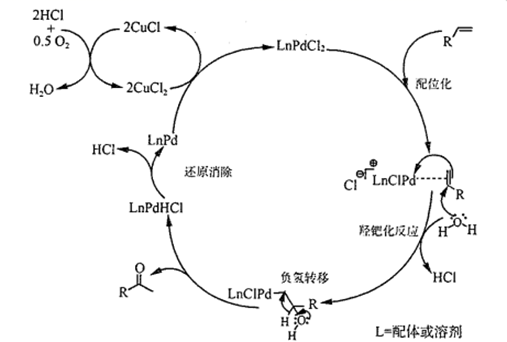


萃取过程为(填“吸热”或“放热”)反应。增大pH会导致萃取率降低的原因是。

A.离子键 B.配位键 C.极性共价键 D.非极性共价键 E. 键 F.
键

其中铁酸钇的化学式为,已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为(
,
-m,
-n),则3号Fe原子的空间坐标为,若晶胞参数分别为a pm、b pm和c pm,阿伏加德罗常数的值用
表示,则该晶体的密度为
(列出表达式)
a.水溶液显酸性
b.遇FeCl3溶液显紫色
c.一定条件下,1mol化合物F最多能与6 mol H2反应
制备
制备NH3(以浓氨水和生石灰为原料):。
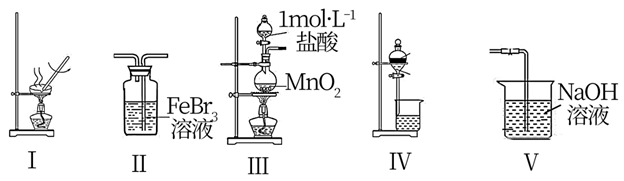
下图所示分别为制备CH4和NH3并得到合适体积比混合气体的装置,根据上述原理选择合适的仪器并连接成装置,则连接顺序为a→e,→f(填接口标号)。装置E中的试剂为(选填“饱和食盐水”、“浓硫酸”或“四氯化碳”)。装置E相当于上述图1装置中的。


实验过程中,采用不同的催化剂,HCN的产率不同,下图所示分别为不同温度,不同催化剂条件下HCN、H2和N2的产率关系图。

由图可知,低温条件下最适宜的催化剂为,高温条件下,选择该催化剂不如另外两种作催化剂时HCN产率高的原因是。

则b极为(填“阴”或“阳”)极,a极的电极反应式为,电解装置中质子交换膜的作用为;若b极产生的O2在一定条件下的体积为336L,a极中通入相同条件下N2的总体积为672L,则N2的转化率为%(保留两位有效数字)。

则各步反应中决定合成氨反应速率的反应方程式为

①平衡曲线上A点的平衡常数 (用含
的式子表示)
②工业实际生产投料时,氮气与氢气的体积比为1:2.8,适当增加氮气的比重的目的是。