
 B .
B .  C .
C .  D .
D . 

①空气常新。空气是一种(选填“混合物”或“纯净物”),其中体积分数为21%的气体是(填写气体的化学式),该气体的用途是。(写一点即可)
②绿水长流。天然水中含有许多杂质,模拟自来水厂净水过程:其中吸附用到的物质是,除去异味、色素或有毒气体等:加氯的作用是。
③能源转型。天然气作为最具潜力的清洁能源,其主要成分是甲烷(CH4),属于(选填“有机”或“无机”)物,0.2mol甲烷分子中约含个碳原子。
|
温度(℃) |
10 |
20 |
30 |
40 |
60 |
80 |
100 |
|
|
溶解度(g/100g水) |
硝酸钾 |
20.9 |
31.6 |
45.8 |
64 |
110 |
169 |
246 |
|
氯化钠 |
35.8 |
36 |
36.3 |
36.4 |
37 |
38.4 |
39.8 |
①从含有80g硝酸钾和9g氯化钠的混合物中提纯硝酸钾,进行如下实验(实验中不考虑各种损耗)
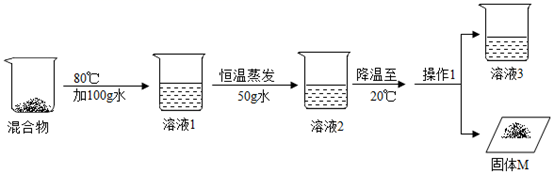
Ⅰ80℃时,硝酸钾的溶解度是。
Ⅱ80℃时,“溶液1”是(选填“饱和”或“不饱和”)溶液。将此溶液恒温蒸发50g水,降温至20℃,所得“溶液3”中硝酸钾的溶质质量分数是。
Ⅲ“溶液2”中硝酸钾质量(选填“<”“>”或“=”)“溶液3”中硝酸钾质量。
Ⅳ若固体M是纯净物,为得到更多固体M,“溶液3”最多还可以恒温蒸发g水。
②20℃时,在100克水中分别放入等质量的硝酸钾和氯化钠,都形成了饱和溶液,如右图所示。

请用两种不同的方法鉴别A和B烧杯中的物质,写出方法、现象与结论。
方法一。
方法二。
①方法一

Ⅰ每步所加试剂均过量的原因是。
Ⅱ写出加入过量NaOH溶液反应的化学方程式。
Ⅲ写出加入过量BaCl2溶液反应的化学方程式。
Ⅳ通过规范的实验操作,甲同学所得的NaCl固体比粗盐样品中的NaCl的质量大,流程中增加NaCl质量的反应有个。
②方法二

Ⅰ提出该方法的同学认为:可用一种试剂X取代方法一中过量NaOH溶液和过量BaCl2溶液,达到提纯NaCl的目的,写出X的化学式。
Ⅱ请依次判断两种方法中所得沉淀的质量关系。
| 沉淀 | 选填“相等”“不相等”或“无法判断” |
| |
|
| BaSO4 |
|
| BaCO3 |
|
②装置B玻璃管中发生的反应为 ,体现出碳的性。
③测定炭粉含量可通过以下两种方法: