 铁丝在氧气中燃烧
B .
铁丝在氧气中燃烧
B .  加热高锰酸钾制氧气
C .
加热高锰酸钾制氧气
C .  电解水实验
D .
电解水实验
D .  过滤
过滤
| A | B | C | D | ||
| X | 氧化物 | 单质 | 混合物 | 纯净物 | |
| Y | 化合物 | 化合物 | 化合物 | 单质 |


| 物质 | a | b | c | d |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
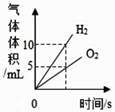 B . 加热高锰酸钾时固体物中锰元素质量变化情况
B . 加热高锰酸钾时固体物中锰元素质量变化情况 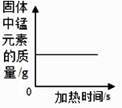 C . 加热氯酸钾和二氧化锰固体混合物时剩余固体质量变化情况
C . 加热氯酸钾和二氧化锰固体混合物时剩余固体质量变化情况 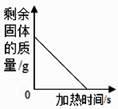 D . 一定质量过氧化氢溶液中加入二氧化锰生成氧气质量的变化情况
D . 一定质量过氧化氢溶液中加入二氧化锰生成氧气质量的变化情况 

A集气瓶事先未先灌满水
B未等气泡连续均匀放出就收集了
C未检查装置气密性

①碳酸钠粉末和稀盐酸 ②锌粒与稀硫酸 ③过氧化氢溶液与二氧化锰
(问题1)铁燃烧时溅落下来的黑色物质中还有没有铁呢?
(查阅资料1)
①自然界中铁易被氧化为Fe3O4和Fe2O3(FeO极易被氧化为Fe2O3)。
②Fe3O4和Fe2O3均能溶于酸的溶液,如盐酸、硫酸等
③铁与酸的溶液反应(如盐酸、硫酸等),有气泡产生。
(实验探究)
将冷却后的黑色物质碾碎,装入试管,加入盐酸溶液,观察到有气泡生成,说明铁燃烧时溅落下来的黑色物质中还含有铁。
(问题2)铁燃烧的产物为什么不是Fe2O3呢?
(查阅资料2)
①Fe3O4和Fe2O3的分解温度、铁的熔点见下表:
|
物质 |
Fe3O4 |
Fe2O3 |
Fe |
|
分解温度/℃ |
1538 |
1400 |
一 |
|
熔点/℃ |
一 |
一 |
1535 |
②Fe2O3高温时分解成Fe3O4
③Fe2O3的颜色为红棕色
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产物是。
①实验中为了防止集气瓶炸裂,必须。
②有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色,就说明包装盒破损进气,这样售货员就能及时发现并处理。
①在D中加热B,生成一种黑色的固体物质;
②C与①的生成物混合,高温下得到B和一种无色气体;
③向①的生成物中通入气体A并加热,得到B和水。
写出实验②的化学方程式:;
写出实验③的化学方程式:。