

| 实验 | 加入的稀硫酸的浓度 | 反应时间 | 收集到的气体/mL | 反应速率 |
| ① | | 15 | 18 | |
| ② | | | 18 | |
| ③ | | | 18 | 12 |
下列说法错误的是( )


①当参加反应的硫粉的质量为g时,发生上述反应放出的热量为 。
②此时生成的气体体积为L(气体已换算成标准状况)。
①已知反应: 。每断裂
键时,该反应放出
的热量,则该反应中的
。在(填“低温”或“高温”)条件下有利于该反应自发进行,判断的依据是。
②在 下,黄铁矿(主要成分为
)的燃烧是工业上制硫酸时得到
的途径之一,
完全燃烧生成
和
时,放出的热量为
,写出
燃烧的热化学方程式:理论上
黄铁矿(
的含量为
,杂质不参与反应)完全燃烧生成
的物质的量为
,转移的电子数为
。

①则上述可逆反应在 内,
。
② 时反应达到平衡,保持温度不变,再往该恒容密闭容器中充入
和
,对于反应
,此时
(填“>”、“<”或“=”)
,判断的依据是。
①
②
③
④
一定温度下,在某恒容密闭容器中充入一定量的 和
,发生反应:
。下列叙述能说明该反应已达到平衡状态的是_______(填标号)。
在 某恒容密闭容器中,充入
和
,发生反应:
。反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
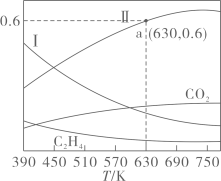
①该反应的 (填“>”或“<”)0,曲线Ⅰ和曲线Ⅱ分别表示(填化学式,下同)和的变化曲线。
②根据图中a点,计算该温度下平衡时的
,
,
的平衡转化率为
(保留三位有效数字)。
③若平衡时a点容器内气体的总压强为 ,则该反应的平衡常数
(列出计算式,用分压表示,分压
总压
物质的量分数)。
若实验中大约要使用80 mLNaOH溶液需要用托盘天平称量NaOH固体g,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和。

①仪器a的名称为。
②(填“能”或“不能”)用相同形状的细铁丝代替仪器a进行实验,理由是。
③反应后生成的溶液的比热容 ,则
溶液和
。稀盐酸发生中和反应的反应热
(已知起始时平均温度为
,反应后最高温度为
,忽略量热计的比热容)。

①做该实验时的环境温度(填“低于”、“高于”或“等于”)22℃。
②该NaOH溶液的物质的量浓度为mol/L。