 B . 铁丝燃烧
B . 铁丝燃烧 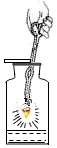 C . 液体加热
C . 液体加热 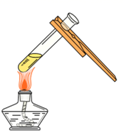 D . 点燃酒精灯
D . 点燃酒精灯 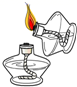
![]()



| 物质 | M | N | P | Q |
| t1时的质量/g | 16 | 50 | 8 | 0 |
| t2时的质量/g | 4 | 18 | x | 44 |
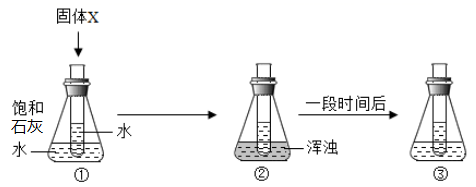

A.石墨 B.一氧化碳 C.干冰 D.甲烷 E.氮气 F.金刚石
a、黄铜 b、不锈钢 c、铁矿石

①a>b ②a<b ③a=b ④均有可能



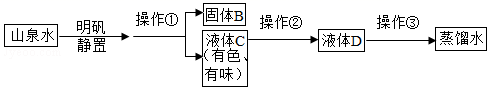
A.漏斗内的滤纸有破损
B.漏斗下端未紧靠烧杯内壁
C.漏斗内液面高于滤纸的边缘
D.滤纸没有紧贴漏斗内壁

①计算:需要氯化钠固体的质量和水的体积。
②称量:用托盘天平称取所需氯化钠固体,放入烧杯中。
③量取:用规格为mL(填“10”、“50”或“100”)的量筒量取所需要的水mL(水的密度为1.0g/cm3),倒入盛有氯化钠的烧杯中;
④溶解:用玻璃棒搅拌,目的是。
经检测,小明同学配制的溶液溶质质量分数偏小,可能的原因是(填序号)。
A.氯化钠固体不纯
B.用生锈砝码称量
C.装瓶时有少量溶液洒出
D.溶解时烧杯内壁有水珠
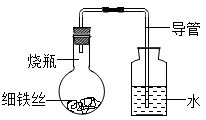
| 烧瓶 | 时间(h) | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A | 干燥的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B | 浸过食盐水的细铁丝 | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C | 浸过清水的细铁丝 | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D | 完全浸没在食盐水中的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
