①固体物质加热后全部变成气体②粮食酿成酒③爆炸④用活性炭除去有毒气体⑤植物的光合作用
 点燃酒精灯
B .
点燃酒精灯
B .  过滤
C .
过滤
C . 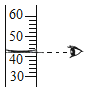 量取液体体积读数
D .
量取液体体积读数
D .  称量NaCl固体
称量NaCl固体
| 原子种类 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 质子数 | 6 | 6 | 8 | 7 | 7 |
| 中子数 | 6 | 7 | 8 | 7 | 8 |
选项 | 事实 | 解释 |
A | 一氧化碟和二氧化碳性质不同 | 分子构成不同 |
B | 金刚石和石墨性质有差异 | 碳原子的结构不同 |
C | 冰水共存物属于纯净物 | 冰水共存物只有水分子 |
D | 湿衣服在阳光下更容易干 | 温度升高,分子运动速率加快 |

| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 3 | 90 | 0 |
| 反应后质量/g | 3.2 | 3 | 待测 | 3.2 |


②3个铵根离子:。
③保持水的化学性质的最小粒子:。
④标出高锰酸钾中锰元素的化合价:。
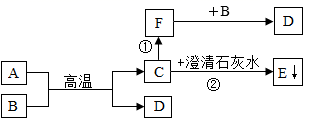
①具有可燃性的气体是。
②有毒的气体是。
③通入紫色石蕊溶液中,溶液变红的气体是。
④能使带火星的木条复燃的气体是。
⑤只能用向上排空气法收集的气体是。
⑥能使灼热的氧化铜还原成铜的固体单质是。
(查阅资料)红磷的着火点为240℃,白磷的着火点为40℃。
(设计实验)同学们设计了如下图所示的方案一和方案二来测定氧气含量。

(进行实验)按上述两个方案进行多次实验。
实验中的磷应该(填“过量”或“少量”),目的是。方案一打开止水夹前观察到的现象为;打开止水夹后观察到的现象为,反应的化学方程式为。
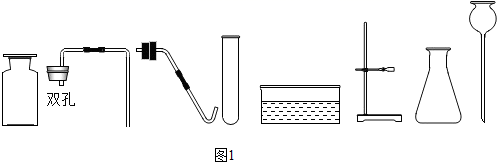
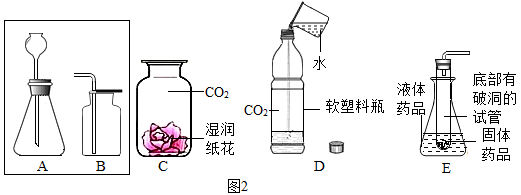
①请连接A和B,将制取装置图补充完整:,反应的化学方程式为,C中的实验现象是。
②D是向装满的软塑料瓶注入约
瓶体积的水,立即旋紧瓶盖,振荡,观察到的现象是。
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 35.9 | 59.8 | 79.7 | 99.7 |
生成氢气的质量/g | 0.1 | x | 0.3 | 0.3 |