 B . 过滤
B . 过滤 C . 氧气验满
C . 氧气验满 D . 倾倒液体
D . 倾倒液体
选项 | A | B | C | D |
实验 |
|
|
|
|
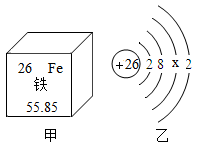
目的 | 比较空气与呼出气体中二氧化碳的含量 | 探究温度高低对分子运动快慢的影响 | 探究铁、铜、银活动性强弱 | 比较铜与黄铜的硬度 |

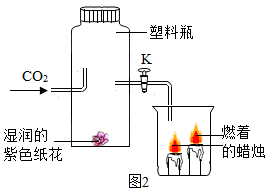
A.收集CO2气体:将CO2气体从n端通入
B.检验CO2是否收满:将燃着的木条放在n端
C.检验所得到的气体是CO2:在瓶中盛少量澄清石灰水,将气体从m端通入
D.测定CO2气体的体积:在瓶中盛满水,m端连接量筒
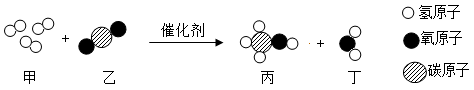
二氧化碳转化为甲醇的化学方程式为。
①可燃冰、天然气的主要成分都是甲烷。请写出甲烷在空气中完全燃烧的化学方程式。为方便贮存和运输,天然气可被压缩到容积很小的钢瓶中,而可燃冰却很难被压缩。试从微观的角度分析可燃冰难被压缩的原因。
②氢气也是一种重要的能源,请设计实验鉴别甲烷和氢气,并完成实验报告。
实验步骤 | 实验现象 | 实验结论 |

①t1℃时,在50g水中加入20g乙固体,充分搅拌后得到(填“饱和或不饱和”)溶液。
②t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须恒温蒸发掉较多水的是(填“甲”或“乙”)物质的饱和溶液。
③使甲物质的溶液状态发生如下改变,对应操作正确的是。
A.a点→c点:加水 B.b点→c点:恒温蒸发
C.a点→b点:升温 D.c点→a点:降温、过滤

【查阅资料】碱石灰能吸收二氧化碳和水蒸气,氢氧化钠溶液能吸收二氧化碳。
【设计实验】
序号 | a | b | c | d |
实验装置 |
|
|
|
|
实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈 |
【得出结论】①说明铜生锈需要水的一组实验是(填实验序号);
②通过实验证明铜与H2O和反应产生“铜绿”。
③碱石灰的作用是。
【查阅资料】氧化亚铜为红色固体,溶于氨水得到蓝色溶液。
【进行实验】实验①,如图1所示实验装置,进行氢气还原氧化铜实验并检验固体产物。

实验②:称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原,其在不同时间(t)所得固体中Cu2O的质量(m)如图2所示。
【实验结论】取实验①反应后的红色固体于烧杯中,加入氨水并搅拌,观察到,证明固体产物有Cu2O。
【进行实验】兴趣小组同学在试管中进行如图3所示的实验,实验中发生反应的化学方程式是:。

实验过程中,小组同学惊奇的发现试管中铝片表面有气泡生成,并收集了该气体。
【提出问题】生成的气体是什么呢?
【猜想与假设】猜想1:可能是SO2;猜想2:可能是H2;……
【实验探究】甲同学用手轻的在盛有该气体的试管口煸动,使极少量的气体飘进鼻孔,发现该气体无气味,认为猜想1不成立,其原因是。乙同学在甲同学实验的基础上,接着进一步实验,验证该气体为H2。
①CuSO4在水中解离出Cu2+和;
②。
铝片和H+会发生如下变化:
【拓展延伸】材料1:硫酸铝溶于水也会发生类似的变化。
材料2:在一定条件下,氢氧化铝具有吸附性,可吸附水里的悬浮杂质。
根据以上信息,请解释硫酸铝也可以用来净水的原因:。
试题篮
0