 B . 加热液体
B . 加热液体 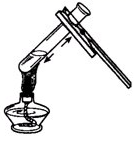 C . 量取液体
C . 量取液体 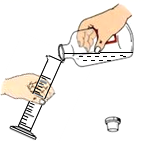 D . 滴加液体
D . 滴加液体 A | B | C | D | |
化学式 | FeO | SO3 | MgCl2 | Ba(OH)2 |
名称 | 氧化铁 | 三氧化硫 | 氯化镁 | 氢氧化钡 |

|
|
|
|
A向一定量的二氧化锰中加入过氧化氢溶液 | B加热一定量的高锰酸钾固体 | C向两份相同的等量稀盐酸中分别加入过量锌粉、镁粉 | D将水通电电解一段时间 |

A.甲、乙两种物质的溶解度相等
B.通过升温可以把甲的饱和溶液变成不饱和溶液
C.t3℃时甲溶液中溶质与溶剂的质量比为60:100
D.将t1℃时甲、乙两种物质的饱和溶液升温至t2℃时(溶剂量不变),所得溶液溶质质量分数关系为甲乙(选填“>”“<”或“=”)。
选项 | 实验目的 | 实验方案 |
A | 除去红墨水中的色素 | 加入足量明矾 |
B | 鉴别碳粉与氧化铜粉 | 取样,分别在空气中灼烧 |
C | 检验二氧化碳 | 将燃着的木条伸入集气瓶中 |
D | 比较铁与铜的活动性 |



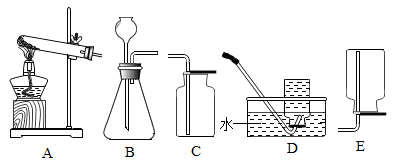
气体 | 制取方法(原理) | 发生装置 | 收集装置 |
氧气 | 1.加热高锰酸钾 | 均可选择(填代号)装置(可根据需要塞入棉花) | 均可选择装置(填代号) |
2.加热氯酸钾与二氧化锰的混合物 | |||
3.固液混合常温反应,化学方程式: | 均可选择B装置 | ||
二氧化碳 | 大理石与稀盐酸常温反应 |

①CD段发生的化学反应方程式为。
②D点压强大于B点,说明反应后容器内压强略大于反应前压强,对此你的解释是。
【查阅资料】①“锡纸”是锡箔或铝箔和纸粘合而成;
②锌粉是一种深灰色固体;
③锡(Sn)与酸或另一种金属的化合物溶液反应时表现为正二价。
【提出猜想】猜想1:“锡纸”中的金属是锡;猜想2:“锡纸”中的金属是铝。
【进行实验】设计方案并进行实验
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 | 猜想成立,反应的化学方程式:。 |
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是。(填代号)
A.氯化钠 B.硝酸银 C.氯化亚铁 D.氯化铜
