⑴酒精 ⑵葡萄糖 ⑶淀粉 ⑷蛋白质
A | B | C | D |
|
|
|
|
聚丙烯 | 聚碳酸酯 | 二氧化氯 | 丁腈橡胶 |
 B . 含14个中子的铝离子:
B . 含14个中子的铝离子:
①向溴乙烷中加入硝酸银溶液,生成淡黄色沉淀,说明含有溴元素 ②蔗糖是最重要的二糖,它的相对分子质量是葡萄糖的二倍 ③聚乙烯、酚醛树脂、纤维素、涤纶、麦芽糖、胰岛素都是合成高分子化合物 ④可以用新制的氢氧化铜悬浊液(可加热)鉴别乙醇、乙酸和葡萄糖 ⑤植物油的主要成分是不饱和的高级脂肪酸 ⑥酿酒过程中,葡萄糖水解得到乙醇 ⑦葡萄糖与果糖互为同分异构体,淀粉与纤维素也互为同分异构体 ⑧甲酸乙酯、麦芽糖、淀粉这三种物质的共同性质是他们既可以发生水解反应,又可以发生银镜反应 ⑨1mol 葡萄糖可与5mol 乙醇发生酯化反应
 的说法,正确的是( )
的说法,正确的是( )


 下列叙述正确的是( )
下列叙述正确的是( )
 可由环氧丙烷和
可由环氧丙烷和 )可由单体
)可由单体 , 1 mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为。
, 1 mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为。

a.均能发生加聚反应 b.只有B能与FeCl3发生显色反应
c.均不能与氢氧钠溶液反应 d.只有C能发生银镜反应
![]()
有机物C9H8O发生如下反应:
![]()
则C9H8O的结构简式为。
已知: ![]()
CH2=CH-CH3(g)+NH3(g)+ O2(g)→CH2=CH-CN(g)+3H2O(g) △H=-514.6kJ·mol-1
i:CH2=CH-CH3(g)+O2(g)→CH2=CH-CHO(g)+H2O(g) △H=-353.1kJ·mol-1
写出反应ii的热化学方程式:。
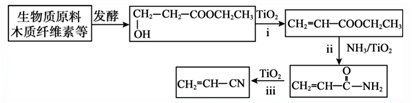
①写出ii的化学方程式:。
②丙烯腈与1,3-丁二烯共聚生产的丁腈橡胶是现代工业重要的橡胶。写出合成丁腈橡胶的化学方程式:。
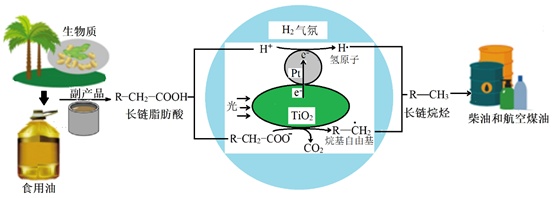
①油脂酸性水解可得高级脂肪酸和(写结构简式)。
②TiO2界面发生的电极反应式为。
①1 molQ最多消耗4 mol NaOH ②核磁共振氢谱有4组吸收峰

请回答:
达喜的化学式是。
 )可制得一种可降解高聚物,该反应的化学方程式是(有机物用结构简式表示)。
)可制得一种可降解高聚物,该反应的化学方程式是(有机物用结构简式表示)。

请回答:
圆底烧瓶中发生的化学反应是( 用化学方程式表示)。

a.升高温度 b.降低温度 c.增加B的起始浓度 d.延长反应时间