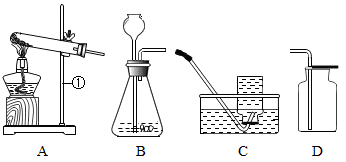
 B . 读取液体体积
B . 读取液体体积 C . 加热液体
C . 加热液体 D . 称量氯化钠固体
D . 称量氯化钠固体

选项 | 实验目的 | 实验操作 |
A | 分离NaCl和泥沙的固体混合物 | 加足量的水溶解,蒸发 |
B | 配制50g质量分数为6%的NaCl溶液 | 向盛有3 g NaCl固体的烧杯中,加入47mL水(密度为1g/cm3),搅拌至充分溶解 |
C | 鉴别固体(NH4)2SO4和NH4Cl | 分别取样,加熟石灰研磨,闻气味 |
D | 除去二氧化碳中的水蒸气 | 通过装有浓盐酸的洗气瓶 |

①贴纸中,熊猫身穿唐代女性的大袖衫。唐代大袖衫由丝绸制作而成,丝绸属于(填“天然”或“合成”)材料。
②身穿秦朝铠甲的金丝猴鼻孔大,上翘,唇厚,无颊囊,这是为了适应高原缺氧进化而来。“高原缺氧”中的“氧”是指(填“氧分子”、“氧元素”或“氧原子”)。

温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
Ca(OH)2 | 0.187 | 0.178 | 0.165 | 0.153 | 0.141 | 0.129 | |




根据实验方案,回答以下问题:
a.加入足量稀硫酸,过滤 b.加入足量硝酸银溶液,过滤 c.在足量氧气中,加热

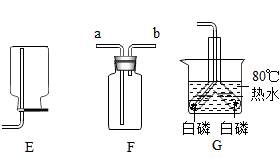
【查阅资料】脱氧剂成分是铁粉、碳粉、碳酸钠、氯化钠;食品干燥剂的成分是生石灰。
【进行实验1】
①取适量脱氧剂于大试管中,加足量的水振荡,充分溶解后过滤,得到滤液A和滤渣甲;
②向滤渣甲中加入足量稀盐酸,观察到有气泡产生,得到黄色溶液,溶液底部有黑色不溶物。
【得出结论1】脱氧剂脱氧的原理是铁粉与发生了化学反应,生成铁锈。
【进行实验2】
①取一包干燥剂放入小烧杯中,加入适量的水,充分搅拌后,用手触摸烧杯外壁,发烫,过滤,得到滤液B和滤渣乙;
②向滤渣乙中加入足量稀盐酸,观察到固体全部溶解,有气泡产生,据此判断滤渣乙中有CaCO3。写出发生反应的化学方程式。
小组同学将上述实验中的滤液A和滤液B倒入废液缸中,观察到有白色沉淀生成,过滤后得到滤液C,他们对C中溶质的成分进行了探究。
【提出猜想】
猜想一:。
猜想二:NaCl、NaOH、Na2CO3;
猜想三:NaCl、NaOH、Ca(OH)2
实验步骤 | 实验现象 | 实验结论 |
步骤1:取少量滤液C于试管中,加入足量氯化钡溶液 | 无明显现象 | 猜想不正确 |
步骤2:继续向步骤1所得溶液中通入二氧化碳 | 有白色沉淀生成 | 猜想三正确 |
①小组同学经过讨论,一致认为根据步骤2的现象不足以证明猜想三是正确的,理由是。
②小林经过认真思考后,对步骤2进行了修改,并做了下面的实验,最终得出了正确的结论,记录如下、请你完善实验报告:
实验步骤 | 实验现象 | 实验结论 |
有白色沉淀生成 | 猜想三正确 |
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量(g) | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 |
充分反应后剩余固体的质量(g) | 24.35 | 23.70 | 23.05 | 23.00 | 23.00 |
根据上表中数据分析,完成下列问题:(写出计算过程)