 B .
B .  C .
C .  D .
D . 
 等质量锌和铁分别与足量的同种稀硫酸反应
B .
等质量锌和铁分别与足量的同种稀硫酸反应
B .  将水通电一段时间后
C .
将水通电一段时间后
C . 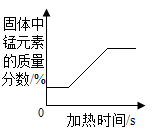 加热一定质量的高锰酸钾
D .
加热一定质量的高锰酸钾
D .  氢气还原一定质量的氧化铜
氢气还原一定质量的氧化铜
A.铁丝 B.硫 C.镁条 D.

A.30℃时,50g水中加入10g固体丙,充分溶解后,所得溶液的质量为60g
B.60℃时,将等质量的甲、乙溶于水形成饱和溶液降温至40℃,溶液中溶剂质量:甲>乙
C.20℃时,甲、乙、丙三种物质的饱和溶液的溶质质量分数:乙>甲>丙
D.40℃时,将甲、乙、丙三种固体分别溶于等质量的水中,都恰好配制成饱和溶液,所得甲、乙、丙的三种物质的饱和溶液的质量由大到小的顺序为
选项 | 实验目的 | 所用试剂或方法 |
A | 用量筒量取5mL水 | 俯视读数 |
B | 验证镁铜银的金属活动性 | 镁、银、硫酸铜溶液 |
C | 使不饱和溶液变成饱和 | 加适量的水 |
D | 软化硬水 |
硫酸铜溶液中的阴离子,锂离子结构示意图,保持甲烷化学性质的最小粒子。

①物质A的化学式为;
②物质C转化成物质B的化学方程式为。



已知:①Ti与TiO2均为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等;②Cl2是一种有毒气体。

①A的化学式为;
②B转化为C的化学方程式是。
①写出A的一种用途;
②C转化成B的化学方程式是。
【查阅资料】
①铜锈俗称铜绿。化学式为Cu2(OH)2CO3 , 受热易分解;
②无水CuSO4为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物。能吸收二氧化碳和水蒸气;
④碳粉不与稀盐酸反应,不溶于稀盐酸;
⑤氧化铜能与稀盐酸反应,溶液变蓝色。
【发现问题】
小组同学将少量铜锈放入试管中加热,发现固体由绿色变成黑色。
【猜想与假设】
猜想一:黑色固体是C粉;
猜想二:黑色固体是CuO;
猜想三:黑色固体是。
实验操作 | 实验现象 | 实验结论 |
取少量样品于试管中,加入足量稀盐酸 | 猜想二正确 |
【进行实验】选择如图所示装置进行验证。

步骤一:连接A和B,打开弹簧夹,通入一段时间的空气;
步骤二:关闭弹簧夹,依次连接装置A→B→(选填“C→D”或“D→C”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热。当观察到,说明铜锈受热分解生成了水。
观察到装置D中澄清石灰水变浑浊,则进一步说明铜锈中一定含有元素。
①装置A的作用是;
②装置D中发生反应的化学方程式为。
