


选项 | 实验操作及现象 | 实验结论 |
A | 把一小块钠放入水中,立刻熔成小球 | 该反应是放热反应 |
B | 向某溶液中加入AgNO3溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
C | 向NaHCO3溶液中滴入酚酞溶液,溶液颜色变红 | NaHCO3溶液显碱性 |
D | 向某溶液中加入NaOH溶液,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色 | 该溶液中一定含有Fe2+ |


①观察到B中的现象是 。
②C中反应后的溶液遇淀粉变蓝,说明Cl2与KI溶液反应生成的物质有。
③D中NaOH溶液的作用是。
④A、B中现象不同,其原因是。

A. B.
B.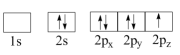
C.![]() D.
D.![]()
A离子键 B.σ键 C.π键 D.氢键
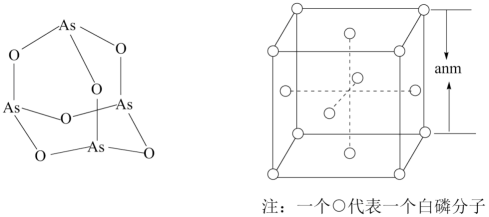

A.离子键B.配位键C.δ键D.范德华力

①Z不能与NaHCO3溶液反应
②Z不能使溴水褪色;
③1molZ与足量金属钠反应可以生成1molH2;
④Z在光照条件下与氯气取代所得一氯取代物只有两种(不考虑立体异构现象)。则Z的结构简式为。