 B . 接种疫苗标志
B . 接种疫苗标志  C . 新冠病毒
C . 新冠病毒  D . 二氧化碳分子
D . 二氧化碳分子 
 B . 检查气密性
B . 检查气密性  C . 滴管用后不洗涤直接插回原瓶
C . 滴管用后不洗涤直接插回原瓶  D . 塞紧橡皮塞
D . 塞紧橡皮塞 

 B .
B .  C .
C .  D .
D . 

 B .
B .  C .
C .  D .
D . 

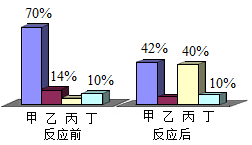
①实验一中若导管口有气泡冒出,则该因素易导致测得的氧气含量偏小;
②实验二需固定左边注射器的活塞,以减小实验误差;
③停止加热后即可读出注射器内气体的体积约为24mL;
④实验取用铜丝质量的多少不会影响实验结果;
⑤实验二全过程中,可观察到注射器内气体的体积一直在减少;
⑥两个实验均能证明空气中约含1/5体积的氧气。其中正确说法的个数有( )



|
物质 |
丙烷 |
氧气 |
水 |
二氧化碳 |
一氧化碳 |
|
反应前质量/g |
4.4 |
12.8 |
0 |
0 |
0 |
|
反应后质量/g |
0 |
0 |
7.2 |
4.4 |
a |





①从b端通入氮气; ②从分液漏斗中滴加适量水;
③从a端通入二氧化碳;④将石蕊溶液染成的紫色的干燥纸花放入广口瓶中;
⑤从a端通入氮气; ⑥从b端通入二氧化碳。
请写出该实验操作(步骤可以重复使用)最合理的顺序是
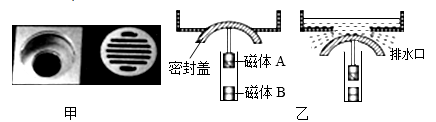
①当密封盖上方无水时,在磁体B作用下,磁体A将密封盖顶起。若磁体A下端为N极,则磁体B上端为极。
②当密封盖上方有水时,密封盖下移,开始排水。积水越多,则排水口越大,其原因是。
|
序号 |
A |
B |
|
实验 装置 |
|
|
|
问题 |
下端木条先熄灭的原因 : 。 |
若用此实验成功验证质量守恒定律,改进的方法是 。 |


【查阅资料】①Cl2是黄绿色、有刺激性气味的气体。②CuCl2在水中解离出 Cu2+、Cl﹣。
【实验二】为了进一步探究CuCl2溶液中哪种离子起催化作用,乙同学做了如图所示的对比实验。那么图中X、Y两个位置填写的数据应该为 、。若要证明CuCl2溶液中的Cu2+对H2O2分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现象为 。
【实验三】丙同学补充如下实验来进一步探究。(提示:CuCl2+2NaOH=2NaCl+Cu(OH)2↓)
|
实验操作 |
实验现象 |
数据处理 |
结论 |
|
向a试管反应后的溶液中加入过量的氢氧化钠溶液 |
有蓝色絮状沉淀产生 |
将沉淀过滤,洗涤,晾干、称量得m2g。则m1、m2的关系为m1=(用m2表示) |
氯化铜反应前后质量未变 |
【查阅资料】①贝壳主要成分为碳酸钙,贝壳中的其它杂质对实验影响可以忽略不计;
②浓盐酸具有挥发性,会挥发出氯化氢气体。
【探究实验一】选择药品
分别取等质量颗粒状和粉末状的贝壳样品与等体积、等浓度的稀盐酸在图1的三颈烧瓶中反应,采集数据,形成如图2和图3的图象。

①对比分析a、b点可知,曲线 (填“①”或“②”)表示颗粒状贝壳与稀盐酸反应;
②对比分析c、d点可知,相同的气压时,与稀盐酸反应速率更快;
③最终粉末状贝壳产生CO2的质量 (填“>”或“<”或“=”)颗粒状贝壳产生CO2的质量。
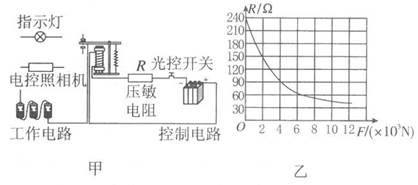
选用图4装置(不包括传感器)制二氧化碳的优点是 ;为了解装置具有该优点的原因,他们在装置中连接压强传感器(如图4左),从而测定实验中试管内气体压强变化的情况(如图4右)。下列说法正确的是 。

A.ab段试管中液面逐渐上升
B.bc段石灰石与稀盐酸脱离接触
C.c点的对应操作是打开弹簧夹
操作步骤:用3个250mL的烧瓶收集满CO2进行实验。如图5所示,同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞;一段时间后,同时振荡三个烧瓶。从左到右依次得到如图6所示的烧瓶内压强与时间的关系曲线1、2、3。
回答下列问题:

曲线2对应发生反应的化学方程式为 ;

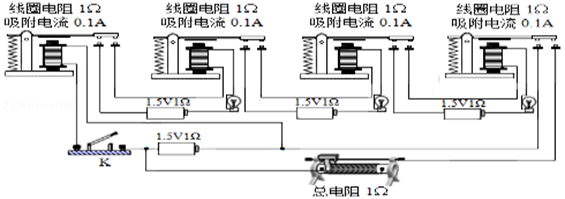
|
操作序号 |
开关及滑动变阻器状态 |
灵敏电流计指针偏转方向 |
|
1 |
开关由断开变为闭合 |
向左 |
|
2 |
开关由闭合变为断开 |
向右 |
|
3 |
开关闭合时,滑片向左移动 |
向左 |
|
4 |
开关闭合时,滑片向右移动 |
向右 |
|
5 |
开关闭合后,滑片不移动 |
不偏转 |
|
6 |
改变电源正负极,闭合开关,滑片向左移动 |
向左 |
|
7 |
改变电源正负极,闭合开关,滑片向右移动 |
向右 |

| 序号 | H2O2溶液的质量/g | H2O2溶液的溶质质量分数 | 植物的器官及质量 | 收集气体的体积/mL | 收集气体的 时间/min |
| 1 | 17 | 15% | 大颗粒胡萝卜16g | 80 | 18 |
| 2 | 17 | 15% | 大颗粒马铃薯16g | 80 | 10.5 |
| 3 | 17 | 15% | 小颗粒马铃薯16g | 80 | 4 |
请依据上述信息分析:
|
实验次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
加入CaCl2溶液的质量/g |
20.0 |
20.0 |
20.0 |
20.0 |
20.0 |
|
反应后溶液的总质量/g |
118.0 |
136.0 |
M |
172.0 |
192.0 |
请根据实验数据分析解答下列问题: