
①晶体中分子间作用力越大,分子越稳定 ②原子晶体中共价键越强,熔点越高 ③干冰是CO2分子通过氢键和分子间作用力有规则排列成的分子晶体 ④在Na2O和Na2O2晶体中,阴、阳离子数之比相等 ⑤正四面体构型的分子,键角都是109°28′,其晶体类型可能是原子晶体或分子晶体 ⑥分子晶体中都含有化学键 ⑦含4.8 g碳元素的金刚石晶体中的共价键的物质的量为0.8 mol
 C .
C . 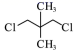

实验目的 | 实验操作 | |
A | 除去乙烷中的乙烯 | 将混合气体通入酸性高锰酸钾溶液 |
B | 除去乙醇中的水 | 加入生石灰,蒸馏 |
C | 鉴别苯和环己烷 | 加入溴水振荡,静置后观察分层及颜色差异 |
D | 分离苯和溴苯 | 加水后分液 |
 ),能改善心脑血管、活血化瘀。有关该化合物的叙述错误的是( )
),能改善心脑血管、活血化瘀。有关该化合物的叙述错误的是( )




①所得与
的配合物中,主要是
与
以个数比
配合所得离子显红色。含该离子的配合物的化学式是。
②铁的另一种配合物铁氰化钾俗称赤血盐,可用于检验
, 两者反应生成带有特征蓝色的沉淀,该赤血盐中心原子的配位数是,请写出一种与其配体互为等电子体的分子。


a.离子键 b.配位键 c.共价键
