A | B | C | D |
|
|
|
|
燃料电池发电站 | 地热发电厂 | 电动汽车充电 | 核能发电站 |
①离子化合物:NaCl、HCl、KOH ②共价化合物:HF、H2S、NH3 ③热稳定性:Na2CO3>NaHCO3
④电解质:ZnCl2、H2SO4、Mg(OH)2 ⑤非电解质:S、CH4、CO ⑥酸性:H2SO4>H3PO4



A.Ba B.Fe C.Br D.Rb
|
元素 |
A |
B |
C |
D |
E |
F |
|
化合价 |
-2 |
+5、-3 |
+4、-4 |
+6、-2 |
+2 |
+1 |
|
原子半径/nm |
0.074 |
0.075 |
0.077 |
0.102 |
0.160 |
0.186 |
写出D元素在元素周期表中的位置。

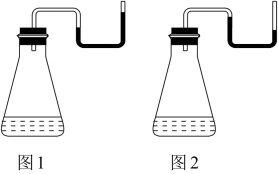
①若如图1所示,发生的反应(假设没有气体生成)是(填“放热”或“吸热”)反应,X可以是(填化学式,只填一种即可)。
②若如图2所示,发生的反应(假设没有气体生成)是(填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是(填字母)。
A.CO还原CuO的反应 B.CaCO3的分解反应 C.Al和Fe2O3的反应

图3
实验中观察到的现象是:大试管中铝片逐渐溶解、有大量气泡产生、烧杯中澄清的石灰水变浑浊,其中“石灰水变浑浊”的主要原因是。