
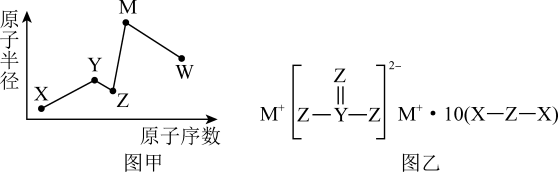



已知:
①Al元素及Si元素在水溶液中的主要存在形式与pH的关系为:

②V2O5为两性氧化物:在水溶液中存在:VO+2H+⇌VO
+H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
价态 | +5 | +4 | +3 | +2 |
存在形式 | VO | VO2+ | V3+ | V2+ |
回答下列问题:
①沉钒率随溶液pH的变化如下图所示。沉钒率随溶液pH值的增加先升高后降低的原因可能是。

②已知25℃时,Kb(NH3·H2O)=1.8×10-5 , Ksp(NH4VO3)=3.0×10-8。若25℃时控制“沉钒”的pH为8.0,当VO恰好完全沉淀时,溶液中的c(NH3·H2O)=mol·L-1。

已知:NaCl、NH4HCO3、NaHCO3、NH4Cl四种盐在不同温度下的溶解度如下表所示:
温度溶解度(g) 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
NaCl | 35.8 | 36.0 | 36.3. | 36.6 | 37.0 | 37.3 | 37.8 |
NH4HCO3 | 15.8. | 21.0 | 27.0 | 一 | 一 | — | — |
NaHCO3 | 8.15 | 9.6 | 11.1 | 12.7 | 14.45 | 。16.4 | 一 |
NH4Cl | 33.3 | 37.2 | 41.1 | 45.8 | 50.4 | 55.2 | 60.2 |
回答下列问题:
I.CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-90.7kJ·mol-l
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-24.5kJ·mol-1
回答下列问题:
温度/K | 400 | 450 | 500 | 550 | 600 | 650 | 700 |
CO转化率 | 22% | 28% | 32% | 40% | 61% | 50% | 18% |
①0~20min内,用CH3OH表示的平均反应速率v(CH3OH)=mol·L-1·min-1;T℃下反应的平衡常数K=。若其他条件不变,向该平衡体系中再充入1molCH3OH和1molCH3OCH3 , 则平衡向(填“正”或“逆”)反应方向移动。
②实验测得该反应:v正=k正c2(CH3OH),v逆=k逆c(CH3OCH3)·c(H2O),k正、k逆为速率常数。若改变温度为Tˊ℃,测得平衡时k正= , 则TˊT(填“大于”或“小于”),判断的理由为。


①能发生银镜反应
②能与钠反应放出H2
③不含-O-O-键,且同一个碳上不连接两个-OH
其中核磁共振氢谱有五个峰的分子的结构简式为。

以甲醇为主要原料设计合成甘油醛(![]() )。
)。