

选项 | 实验目的 | 所用试剂或操作方法 |
A | 鉴别NaOH、CaCO3、NH4NO3三种白色固体 | 分别取样与试管中,加入适量水,搅拌 |
B | 提纯混有少量KNO3的NaCl | 高温溶解、冷却结晶、过滤 |
C | 鉴别溶液:氯化钡溶液、氢氧化钠溶液、硫酸钠溶液、氯化铵溶液 | 不用其它试剂,将四种溶液分别取样,两两相互滴加,观察现象 |
D | 除去NaCl溶液中混有的少量Na2CO3 | 加过量CaCl2溶液,过滤 |
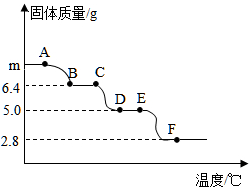
 向AgNO3和Cu(NO3)2中混合溶液中加入锌粉至过量
B .
向AgNO3和Cu(NO3)2中混合溶液中加入锌粉至过量
B .  常温时向一定量的Ca(OH)2溶液中通入CO2至过量
C .
常温时向一定量的Ca(OH)2溶液中通入CO2至过量
C .  向一定质量的氢氧化钠和氯化钡的混合溶液中逐滴加入稀硫酸至过量
D .
向一定质量的氢氧化钠和氯化钡的混合溶液中逐滴加入稀硫酸至过量
D .  向等质量、溶质质量分数相同的稀盐酸中分别逐渐加入镁粉和铁粉至过量
向等质量、溶质质量分数相同的稀盐酸中分别逐渐加入镁粉和铁粉至过量

【查阅资料】
①Cu2(OH)2CO3与盐酸反应生成氯化铜、水和二氧化碳。
②铁能与氯化铁溶液反应,化学方程式为2FeCl3+Fe=3FeCl2
③氢氧化亚铁易被氧气氧化,化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3下列说法错误的是( )




①发生装置应选用(填字母)。
②KCl的溶解度曲线如下图所示。将反应后的残余固体冷却至室温,加足量水溶解后过滤,滤渣经处理得到MnO2。从滤液中获得KCl晶体的最佳方法是。


【查阅资料】Na2SO4、NaCl溶液呈中性
猜想Ⅰ NaCl、Na2SO4
猜想Ⅱ NaCl、Na2SO4和。
猜想Ⅲ NaCl、Na2SO4和H2SO4
猜想Ⅳ NaCl、Na2SO4、H2SO4、Na2CO3
实验步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液 | 猜想Ⅲ正确 | |
方案二 | 取少量烧杯中的溶液于洁净的试管中,加入少量铁粉 |
【反思与总结】分析反应后溶液中溶质成分除要考虑生成物,还需考虑反应物是否过量。
