选项 | 劳动项目 | 化学知识 |
A | 学农活动:在田地里施洒KNO3 | KNO3属于复合肥 |
B | 学校清洁:用酒精对课桌椅进行消毒 | 酒精可燃烧 |
C | 社区服务:垃圾分类,植树造林 | 节约资源,低碳环保 |
D | 家务劳动:用洗洁精洗碗碟 | 洗洁精有乳化作用 |
 B . 处理废弃药品
B . 处理废弃药品 C . 滴加液体
C . 滴加液体 D . 倾倒液体
D . 倾倒液体
 )画出奥运五环,把甲基橙滴入乙酸溶液变出红色环,滴入碳酸钠溶液变出黄色环。下列说法正确的是( )
)画出奥运五环,把甲基橙滴入乙酸溶液变出红色环,滴入碳酸钠溶液变出黄色环。下列说法正确的是( )

选项 | 实验目的 | 实验操作 |
A | 鉴别NH4Cl和(NH4)2SO4固体 | 分别加入熟石灰研磨,闻气味 |
B | 检验固体中是否含有 | 取样,加入稀盐酸观察是否有气泡产生 |
C | 鉴别氢气和甲烷 | 分别点燃,在火焰上方罩干冷烧杯 |
D | 检验集气瓶中氧气是否集满 | 将带火星的木条放在瓶口,观察是否复燃 |

实验前的体积 | 实验后的体积 | |
锥形瓶内空气(含导管内空气) | 烧杯内水 | 烧杯内剩余水 |
246.0mL | 100.0mL | 51.5mL |
下列说法不合理的是( )

①如图为钛原子结构示意图,则x=。
②用过量的镁在加热条件下与TiCl4发生置换反应制得金属钛,其化学方程式为。
③钛合金可能具有的性质是(填标号)。
A.密度大,强度高 B.熔点高,密度小 C.耐腐蚀,硬度小




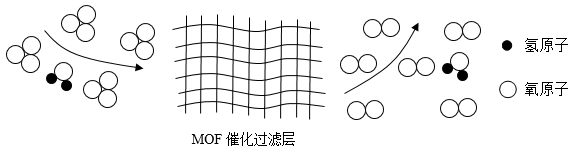
①反渗透过程属于(填“物理变化”或“化学变化”)。
②检验所得纯净水含较少钙、镁离子的操作和现象:。

①当温度低于2000℃时,体系内微粒含量没有改变的原因是。
②已知图中曲线A、B对应的微粒是原子,写出微粒A的化学符号。

①乙的化学式是。
②写出乙→丙的化学方程式:。
①丙的化学式是。
②写出乙→丙的化学方程式:。

已知高铁酸钾部分性质如下:
ȋ.热稳定性差,在低温、碱性环境中稳定;
ⅱ.在水中溶解度大,难溶于无水乙醇等有机溶剂。

取150mL蒸馏水和150mL溶质质量分数为3%、2%、1%的氢氧化钠溶液于4个烧杯中,分别加入20g干冰,通过传感器测其pH,且pH变化如图2所示。

用NaOH固体配制一定溶质质量分数的溶液,无需用到的仪器有____(填标号)。
在密闭体系中,分别往等体积、等浓度的Na2CO3溶液和NaHCO3溶液逐滴加入等浓度的稀硫酸,压强变化曲线如图3所示。

0~50s,压强无明显变化的体系中,反应生成的含碳元素的盐类物质M是(填化学式)。
实验编号 | A | B | C |
取20mL对应溶液 | 3%NaOH与干冰反应后的溶液 | 2%NaOH与干冰反应后的溶液 | 1%NaOH与干冰反应后的溶液 |
完全生成M时消耗硫酸体积V1/mL | 4.14 | 1.43 | 0.36 |
M完全转化成CO2时消耗硫酸体积V2/mL | 4.55 | 2.46 | 1.60 |
①结合表中数据分析,2%NaOH与干冰反应后溶液中的溶质是。
②所取的20mL溶液中,Na2CO3质量分数最大的是(填实验编号)。