 B .
B .  C .
C .  D .
D . 
| A.物质的分类 | B.物质的检验 |
| 合成橡胶、合金和合成纤维都是合成材料 冰水、雨水和矿泉水都是混合物 消石灰、纯碱和烧碱都是碱 | 用湿润的蓝色石蕊试纸能检验氨气 用灼烧的方法能区别棉花和羊毛 用适量的水能区分NH4NO3固体和NaCl固体 |
| C.化学生产 | D.化学历史 |
| 工业上可以用煤经过干馏制得煤焦油 使用热固性塑料制电器插座 用聚氯乙烯塑料袋制食品包装袋 | 拉瓦锡通过定量实验证明了化学反应遵循质量守恒的结论 汤姆森首先发现了电子,证实原子是可分的 俄国化学家门捷列夫将当时已发现的63种元素推序,制得了第一张元素周期表 |

| 序号 | 物质 | 杂质 | 试剂 | 操作 |
| A | Fe | Fe2O3 | 盐酸 | 结晶 |
| B | NaCl | NH4HCO3 | — | 加热 |
| C | Cu(NO3)2溶液 | BaCl2 | AgNO3溶液 | 过滤 |
| D | CO2 | 水蒸气 | 生石灰 | 洗气 |

 B . 向一定量的氯化钡和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量
B . 向一定量的氯化钡和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量  C . 电解水
C . 电解水  D . 向盛有一定量稀盐酸的烧杯中不断滴入NaOH溶液至过量
D . 向盛有一定量稀盐酸的烧杯中不断滴入NaOH溶液至过量 
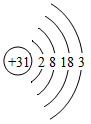 ,形成的氧化物化学式表示为。
,形成的氧化物化学式表示为。 ②下列原子结构示意图所对应的元素与镓元素的化学性质相似的是(填字母序号)。

金属镓能与稀盐酸反应。写出反应的化学方程式。
①根据图中的相关信息,下列对镉元素的判断错误的是。
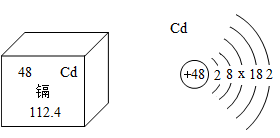
A.镉属于金属元素 B.一个镉原子中有48个质子
C.镉原子示意图中X=8 D.镉的相对原子质量为112.4g
②“镉大米”主要出现在河水、土壤遭到镉污染的地区,消除“镉大米”需要从源头治理。目前河水治理的方法是:把适量Na2CO3投入被Cd2+”污染的河水中,形成沉淀,以降低河水中Cd2+”的浓度。若某河段主要含有氯化镉,写出与碳酸钠反应的化学方程式为。
|
物质 |
甲 |
乙 |
丙 |
丁 |
|
| 化学式 | H2O | C | ? | H2 | |
| 微观 示意图 | | | | ? |

A是40℃含有120g水的甲溶液,经过如图2操作,得到50g甲固体。对以上过程的分析,错误的是______(选填编号)

阅读资料:a.青蒿素 无色针状晶体,味苦。在丙酮、醋酸乙酯、氯仿、苯及冰醋酸中易溶,在乙醇和甲醇、乙醚及石油醚中可溶解,在水中几乎不溶。熔点:156-157℃,而青蒿素在温度超过60℃以后则过氧桥结构被很快破坏,完全失去药效;
b.乙醚 化学式为C4H10O,无色透明液体。有特殊刺激气味。带甜味,极易挥发,其蒸汽重于空气。易燃、低毒,与无水硝酸、浓硫酸和浓硝酸的混合物反应也会发生猛烈爆炸,熔点 -116.3℃。沸点 34.6℃;
c.乙醇 是一种有机物。俗称酒精。在常温、常压下是一种易燃、易挥发的无色透明液体,沸点是78.3℃,熔点是-114.1℃,易燃,其蒸气能与空气形成爆炸性混合物,能与水以任意比互溶。
请回答:

①滤渣的主要成分是(填化学式);
②盐酸酸化,其目的之一是除去未反应的氢氧化钙,写出反应的化学方程式。
①若要达到排放标准,可以向废水里加入(填序号)。
A.氯化钠 B.氯化钡 C.生石灰
②某同学欲利用该村的赤铁矿(杂质不溶于水,也不与酸反应)来处理废水,并制取红色颜料(Fe2O3)从而变废为宝。他设计了如下方案,试回答相关问题。

写出反应③的化学方程式。
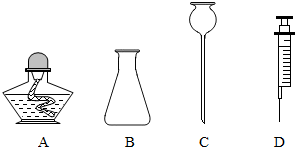
不能用排空气法收集乙烯的原因是。

①先如图A表示,收集一瓶乙烯体积分数为50%的混合气体,点火不发生爆炸,
②再如图B、C所示,分别收集气体并点火,前者发生爆炸,后者不爆炸,结合步骤①,得出a%、b%的范围,其中b%的范围是:%—%。
③按照中值法继续探究,可得到更准确的爆炸极限数据。
④启示与感悟:小明同学在完成“氧气的制取与性质”的基础实验后,他还想进行蜡烛在不同浓度的氧气中燃烧情况的探究,现要较简便地获得两瓶不同浓度的氧气,应选择收集氧气的方法是。实验室制取氧气方法较多,写出比较环保、安全的反应化学方程式。
|
实验次数 |
1 |
3 |
4 |
5 |
6 |
|
取样品质量(g) |
25.0 |
25.0 |
25.0 |
25.0 |
25.0 |
|
取稀盐酸质量(g) |
50.0 |
120.0 |
140.0 |
160.0 |
205.0 |
|
产生气体质量(g) |
0 |
a |
2.2 |
3.3 |
4.4 |