①NO(g)+Br2(g)=NOBr2(g) △H1快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2慢反应。
下列说法错误的是( )

用0.1mol 配成稀溶液与足量稀硝酸反应,能放出kJ的能量。

的平衡转化率
%,反应平衡常数K=。
T/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
①写出化学平衡常数K的表达式。
②试比较K1、K2的大小,K1K2(填“>”、“<”或“=”);
③400℃时,反应2NH3(g)N2(g)+3H2(g)的化学平衡常数为。当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正v(N2)逆(填“>”、“<”或“=”)。
①:。
②:。
①向等体积、等浓度的盐酸和醋酸溶液中加入大小相同的镁条,开始时反应速率分别为v1、v2 , 其大小关系为。
②等体积、等pH的盐酸和醋酸溶液分别与足量的等浓度的NaOH溶液反应,消耗NaOH溶液的体积分别为a、b,其大小关系为。
①在相同条件下,试比较、
和
酸性从强到弱顺序为。
②向溶液中加入足量
溶液,反应的离子方程式为。
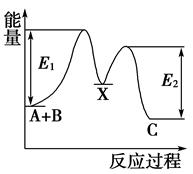
CO还原法:一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,每生成16gS(s),该反应(填“放出”或“吸收”)的热量为。

①
②
③
Ⅰ.CO的燃烧热为。若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为kJ。
Ⅱ.CO将NO2还原为单质的热化学方程式为。