
下列有关说法错误的是( )

选项 | 反应 | 甲 | 乙 |
A | 外形、大小相近的金属和水反应 | ||
B |
|
|
|
C |
| 热水 | 冷水 |
D |
| 无 | 加 |
A | B | C | D |
|
|
|
|
Cu-Zn原电池 | 粗铜精炼 | 铁片镀锌 | 验证NaCl溶液(含酚酞)电解产物 |

|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
|
|
|
|
|
|
|
内该反应的平均速率
。

①
②
写出气态肼和生成氮气和水蒸气的热化学方程式。
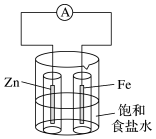
锌棒上发生的电极反应为;铁棒上发生的电极反应为。
实验Ⅱ中电流表指针的偏转方向与实验Ⅰ(填“相同”或“相反”)。
用(填仪器名称,下同)量取食用白醋,在烧杯中用水稀释后转移到
容量瓶中定容,摇匀即得待测白醋溶液。
![]()
滴定次数 | 1 | 2 | 3 | 4 |
| ||||
|
(Ⅲ)数据处理与讨论
甲同学在处理数据时计算得:平均消耗的溶液的体积
, 乙指出其计算不合理。按正确数据处理,
;该市售白醋的总酸量
。

请回答下列问题: