 B .
B .  C .
C .  D .
D . 
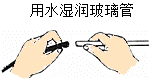 B . 检查装置气密性
B . 检查装置气密性  C . 塞橡胶塞
C . 塞橡胶塞 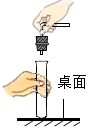 D . 闻药品气味
D . 闻药品气味 
| ①喷稀醋酸 | ②喷水 | ③直接放入CO2中 | ④喷水后放入CO2中 |
| 组别 | 实验方案或仪器用品 | 实验目的 |
| A | 带火星的小木条 | 鉴别二氧化碳和氧气 |
| B | 加肥皂水,观察泡沫、浮渣 | 鉴别软水和硬水 |
| C | 分别点燃,在火焰上方罩一个干冷的烧杯,观察现象 | 鉴别H2和CH4 |
| D | 将铜丝伸入溶液中 | 鉴别硝酸银溶液和稀盐酸 |



①钪的相对原子质量为,钪离子的符号为。
②图2所表示的四种粒子中,与钪原子的化学性质相似的是(填字母)。


①仪器a的名称是。
②调平天平后,将铁钉从天平托盘上转移到仪器a的溶液中,一段时间后可以观察到铁钉表面出现,发生反应的化学方程式为。
③实验过程中,天平指针始终没有发生偏移,这可以说明在发生化学反应前后,各物质的。
①通过甲装置中的铜片上红磷和白磷的变化现象对比,可以得出有关燃烧发生的条件是。
②用丙装置进行实验时,可观察到水槽内壁上的水位高低变化情况是。
③甲和丙相比,丙更适合作为密闭教室的演示实验装置,原因是。
④以下对三组实验进行的分析或总结中,错误的是。(填字母序号)
a、三组实验中小烧杯里的热水都只起提高温度的作用
b、甲、丙两组实验都应用了“对比实验”的研究方法
c、若将乙组中白磷换成红磷,也能观察到燃烧现象
经交流讨论,小组一致认为肯定不是氧化钙。小组得出这一结论的理由是(用化学方程式表示)。
②生产碳化钙的原料是碳酸钙,所以碳化钙中常有没反应完全的碳酸钙。
(做出猜想)小组经过讨论,对白色固体的成分提出如下几种猜想:
猜想Ⅰ:Ca(OH)2; 猜想Ⅱ:CaCO3; 猜想Ⅲ:。
|
实验操作 |
实验现象 |
|
a、取少量白色固体放入烧杯中,加入蒸馏水,振荡静置,取上层澄清溶液于试管中,通入CO2 |
溶液变浑浊 |
|
b、另取少量白色固体放入烧杯中,加入足量稀盐酸 |
无气泡产生 |
操作a中通入CO2时,发生反应的化学方程式为。
由操作b的实验现象分析,白色固体中没有。


| 实验编组 | 等质量稀硫酸 | 金属粉末质量/种类 | 对应曲线 |
| ① | 含H2SO49.8g | 6.5g/镁 | a |
| ② | 含H2SO49.8g | 6.5g/锌 | b |
| ③ | 含H2SO49.8g | 6.5g/铁 | c(待绘制) |