①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸

①氯水、②碳酸钠晶体、③烧碱、④漂白粉、⑤过氧化钠、⑥碳酸氢钠
①取适量溶液,加入足量NaOH溶液,生成白色沉淀。
②过滤,向滤液中加入足量溶液,有白色沉淀生成。根据上述实验回答下列问题。


①写出E中发生反应的化学方程式:。
②资料表明E中的产物有以下性质:
a.受热易升华,冷却后易凝华;b.遇剧烈反应。
为收集E中的产物,在E与F之间增加一个收集装置,同时将装置F换成了装置G,则G的两个作用是、。
已知1个在反应中得到6个电子生成X,则X的化学式为。

回答下列问题:
在下列化学方程式中用双线桥法标出电子转移的方向和数目:
a.均属于电解质 b.溶于水立即加入酚酞试液最终均为红色
c.均能通过化合反应一步生成 d.溶于水均伴随着放热现象
实验1:加热碳酸氢钠固体,装置如下图所示。
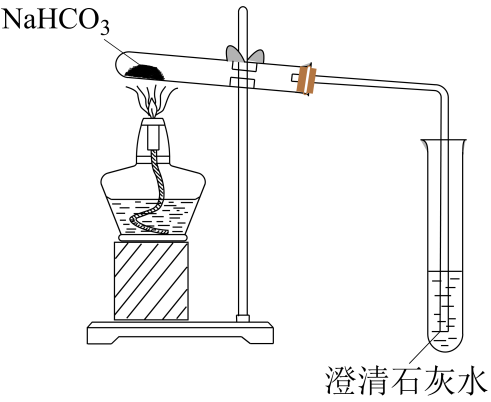
①利用上述装置可实现向
的转化,被加热的试管中发生反应的化学方程式为。
实验2:分别向滴有2滴酚酞的和
溶液中滴加稀盐酸,实验记录如下:
实验内容 | 实验现象 |
实验2-1 | 溶液浅红色褪去,立即产生大量气泡。 |
实验2-2 | 开始时,溶液的红色没有明显变化,电没有明显的气泡产生。继续滴加盐酸,当溶液的红色明显变浅时,气泡的数量血逐渐增多。当溶液的颜色变为浅红色,继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现。 |
②实验2-1中,反应的离子方程式是。
③实验2-2中,实现碳酸钠向碳酸氢钠转化的现象是,反应的化学方程式:。
④碳酸也可实现上述转化,写出将通入
溶液中发生反应的离子方程式:。