 B . 取用固体
B . 取用固体 C . 加热液体
C . 加热液体 D . 加热固体
D . 加热固体





选项 | 实验目的 | 实验方案设计 |
A | 鉴别CO2和CO | 闻气味 |
B | 干燥的紫色石蕊纸花 | |
C | 除去CO2中的少量CO | 通过灼热的氧化铜 |
D | 用燃着的木条点燃 |


①横坐标的时间表示的是加热时间
②反应的氯酸钾的质量大于高锰酸钾的质量
③曲线c表示氧气的质量随时间的变化
④高锰酸钾不是氯酸钾分解的催化剂
⑤t3时,剩余的固体物质有四种
⑥起催化作用的物质的质量逐渐增多至不变



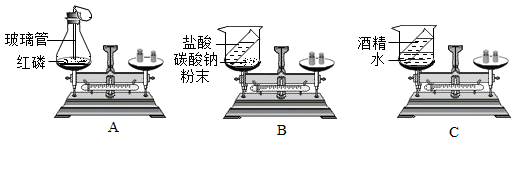
如图所示的三个实验中,遵守质量守恒定律的是(填序号)。
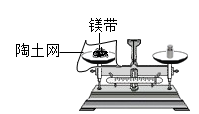
①镁带与空气中燃烧的化学方程式为。
②小卓认为根据质量守恒定律,天平应该向左倾斜。等到镁带完全燃烧后,发现天平向右倾斜,请分析其主要原因是。


【查阅资料1】常温下没有氧气存在时,铁与水几乎不反应,但高温下铁与水蒸气能反应,生成一种固体和一种气体。

猜测Ⅰ:氧气 猜测Ⅱ:氢气 猜测Ⅲ:二氧化硫
小红认为不需要做实验就可以排除猜想Ⅲ,她的理由是。
同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”。玻璃管内的黑色固体中还可能含有“剩余的铁”。
【查阅资料2】
①铁的氧化物有三种:FeO、Fe2O3、Fe3O4 , 其中仅有Fe2O3为红棕色,FeO、Fe3O4均为黑色,但FeO一接触到空气会立即变成红棕色。
②铁的三种氧化物都不与硫酸铜溶液反应,铁能与硫酸铜溶液反应生成红色物质。
【实验探究】
①将玻璃管中的黑色固体倒出,平铺于白纸上,没有发现红棕色的物质,一会儿之后黑色固体也不变色,则黑色固体中一定没有(填物质名称)。
②取上述黑色固体少许加入足量的硫酸铜溶液,发现(填实验现象),说明黑色固体中一定有铁和四氧化三铁。
【实验结论】铁与水蒸气发生反应的化学方程式为。