 B .
B .  C .
C .  D .
D . 
 B .
B . 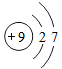 C .
C . 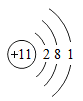 D .
D . 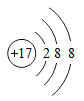



选项 | 实验目的 | 实验现象 | 实验结论 |
A | 探究同种物质在不同溶剂中的溶解性 | 试管①中固体溶解,试管②中固体不溶解 | 温度和溶剂质量相同时,氯化钠在水中比在汽油中更易溶解 |
B | 验证质量守恒定律 | 烧杯中产生大量气泡,托盘天平指针向右偏转 | 该化学反应不遵循质量守恒定律 |
C | 探究水的组成 | 火焰呈淡蓝色,烧杯内壁有水雾出现 | 水由氢元素和氧元素组成 |
D | 探究二氧化碳与氢氧化钠溶液的反应 | 两个烧瓶中的气球都鼓起来,且烧瓶①中气球明显大于烧瓶②中气球 | 二氧化碳能与氢氧化钠溶液发生反应 |
 用过氧化氢溶液和二氧化锰制取氧气
B .
用过氧化氢溶液和二氧化锰制取氧气
B .  质量相等的镁和氧气在点燃的条件下充分反应
C .
质量相等的镁和氧气在点燃的条件下充分反应
C .  向 pH=13 的某碱溶液中不断加水
D .
向 pH=13 的某碱溶液中不断加水
D .  向一定量NaOH 和 Ba(NO3)2的混合溶液中加入稀硫酸
向一定量NaOH 和 Ba(NO3)2的混合溶液中加入稀硫酸

2022 年 12 月 4 日,神舟十四号载人飞船返回舱在东风着陆场成功着陆,标志着 183 天的神舟十四号载人飞行任务取得圆满成功。
航天员长期驻留空间站从地球运送物资到太空成本太高,因此要尽可能实现空间站物资的循环使用。我国空间站的再生式环控生保系统,共包括 6 个子系统。其中电解制氧子系统等 5 个子系统已实现了空间站氧气、水等资源的再生利用。神舟十四号航天员在地面人员的配合下,完成了二氧化碳还原子系统的组装和测试,即将舱内收集起来的二氧化碳与电解水产生的氢气反应,再次获得水。
航天强国建设,正以势不可挡的步伐汇入中国式现代化建设的伟大事业中。




①写出仪器x 的名称:。
②实验室可用石灰石和稀盐酸反应制取二氧化碳,写出其发生反应的化学方程式。可选用的发生装置为(填字母序号)。选择收集装置需要考虑的因素有。

①若要证明b 处二氧化碳与水发生反应生成碳酸使紫色石蕊溶液变红,可在 a 处放置做对照实验。
②写出 c 处发生反应的化学方程式。
③实验过程中观察到烧杯内下层蜡烛先熄灭,上层蜡烛后熄灭,由此推断二氧化碳具有的性质有。

甲同学设计如下探究方案。
|
实验方案 |
实验现象 |
实验结论 |
|
方案一:将打磨过的光亮铁钉放入试管中,倒入少量该无色溶液。 |
|
该溶液是稀盐酸 |
|
方案二:另取少量无色溶液于试管中,加入少量某种盐溶液,该盐溶液中的溶质为(填化学式) |
产生大量无色气泡 |
常温下,向盛有 100g 溶质质量分数为 4%的氢氧化钠溶液的烧杯中逐滴加入上述稀盐酸,用 pH 传感器测得溶液的 pH与所加稀盐酸质量的变化曲线如图所示。

①该化学反应的微观实质是。
②当溶液为中性时,消耗稀盐酸的质量为g。
③计算该稀盐酸的溶质的质量分数(写出具体计算过程)。
部分流程如下:

操作 1 的名称是。
用粗盐(含CaCl2、MgCl2、Na2SO4、泥沙等杂质)制氢氧化钠的流程如下:

步骤①②③中的试剂添加顺序还可以是(填序号)。