 )分子中所含的共价键数目为6
)分子中所含的共价键数目为6Mn(VII)Mn(VI)
Mn(IV)
Mn(III)
[Mn(C2O4)n]3-2n→Mn2++CO2
下列说法错误的是( )
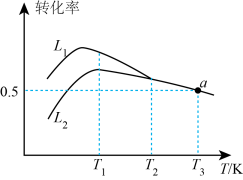
①线(填“L1”或“L2”)表示丙烷的转化率。
②温度高于T1K后曲线L2随温度升高而降低的原因为。
③当温度高于(填“T1”或“T2”)时,可判断反应ii不再发生,a点对应的温度下,丙烯的分压p(C3H6)=kPa(保留3位有效数字,下同),反应i的平衡常数。(已知:分压p分=总压×该组分物质的量分数,对于反应
,
, 其中
、
、
、
为反应平衡时各组分的分压)

已知三步反应的活化能:反应I>反应III>反应II。则催化过程的决速反应为(填“反应I”“反应II”或“反应III”)。
①
②
③
计算热分解反应④
的
。

①越小,
平衡转化率,理由是。
②对应图中曲线,计算其在
之间,
分压的平均变化率为
。
Ⅰ.取已知浓度的溶液,搅拌下滴加足量
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸()溶液中加入适量
固体,制得
和
混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80~85 ℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:

反应Ⅰ:![]() (g)
(g)
反应Ⅱ:
乙烯与在a、b两种催化剂作用下发生反应,催化剂的催化活性(用EO%衡量)及生成EO的选择性(用EO选择性%表示)与温度(T)的变化曲线如图一所示。

①依据图给信息,选择制备环氧乙烷的适宜条件为。
②M点后曲线下降的原因为。
③下列说法正确的有(填标号)。
A.催化剂的选择性越高,其达到最高反应活性所需的温度越高
B.催化剂的催化活性与温度成正比
C.不同催化剂达到最高活性时的温度不同

①0(填“>”或“<”)。
②在T℃的恒温、恒容密闭容器中,按体积分数充入反应混合气体:乙烯30%、氧气7%,其余混合气63%(致稳气),发生反应Ⅰ(忽略反应Ⅱ)。平衡时体系压强为2000kPa,乙烯的转化率为 , 则T℃下反应Ⅰ的相对压力平衡常数
。
科学家利用、水合成环氧乙烷,有利于实现碳中和。总反应为:
![]()
, 该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。

①电解槽1中阴极的电极反应式为。
②图四虚线框中发生的反应为:、、
。