


首先将含有NaF和FePO4各0.025mol的原料研磨混合30min,混合均匀转移到80mL。的水热釜中,将0.025mol的CH3COONa溶于6mL蒸馏水中,并加入1g蔗糖溶解均匀并慢慢加入水热釜中得到流变态混合物,请回答下列问题:
①(NH4)2Fe(SO4)2+2H2O+H2C2O4=FeC2O4·2H2O↓+(NH4)2SO4+H2SO4
②6FeC2O4·2H2O+3H2O2+6K2C2O4=4K3[Fe(C2O4)3]+2Fe(OH)3↓+12H4O
③2Fe(OH)3+3H2C2O4+3K2C2O4=2K3[Fe(C2O4)3]+6H2O

①实验中加入2~4滴3mol/LH2SO4的目的是;
②用蒸馏水洗涤沉淀的具体操作为。

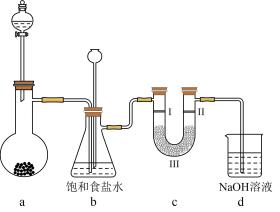
①仪器a的名称是,反应保持为40℃的原因是;
②逐滴加入H2O2和H2C2O4的目的是,为了达到该目的,还可以进行的实验操作为。
①加入高锰酸钾溶液时发生反应的离子方程式为。
②该样品的质量分数为(写出表达式即可),测量值比实际值偏小,原因可能是(任写一种即可)。
已知:C(s)+O2(g)⇌CO(g) △H1=-110.5kJ/mol ①
C(s)+CO2(g)⇌2CO(g) △H2=+552.5kJ/mol ②
工业上将一定比例的氧气和二氧化碳投入焦炭炉中反应,不同温度下,达到平衡时氧气和二氧化碳体积分数如图:

试解释随温度的升高氧气与二氧化碳的变化趋势的原因:;在850℃时反应炉中达到热平衡,则通入的n(O2):n(CO2)=(填,最简单整数比);此时反应器中压强为p0 , 则反应②的Kp=。

则曲线c表示的物质是;e点CO的转化率为;(用分数表达或保留三位有效数字)在M点平衡状态下进行压缩,则重新达到平衡,M点可能移到:。(填“不变”“O”“N”或“P”)。

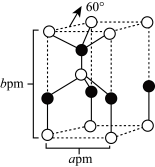

试剂1:;试剂2:;产物1:。