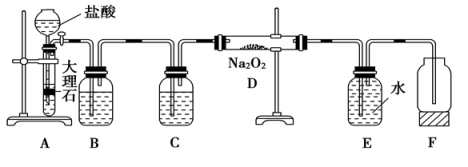
①NaOH固体溶于水能导电,所以NaOH是电解质
②CO2的水溶液能导电,所以CO2是电解质
③液态铜的导电能力很强,所以铜是电解质
④FeCl3溶液能导电,所以FeCl3是电解质
⑤C2H5OH(乙醇)是化合物,所以它是电解质
⑥BaSO4、CaCO3都是难溶物,其水溶液不导电,故它们不是电解质
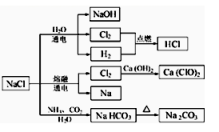
| X | Y |
| Z | W |
①含有金属元素的化合物一定是离子化合物 ②第ⅠA族和第ⅦA族原子化合时,一定生成离子键
③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物 ⑥离子化合物中可能同时含有离子键和共价键.
①CO2 ②HCl ③H2O ④O2
以上物质中属于混合物的是(填序号,下同),属于电解质的是。
①将部分粉末加入水中,振荡,有白色沉淀生成;
②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
③取少量②的溶液滴入溶液,有白色沉淀生成.
根据上述实验现象,判断原白色粉末中肯定含有,可能含有,并写出有关反应的离子方程式。(写两个即可)

A.称量时用了生锈的砝码;
B.将NaOH放在纸张上称量;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中(假设:溶液的热胀冷缩程度大于容器)
D.往容量瓶转移时,有少量液体溅出;
E.定容时俯视刻度线;
F.容量瓶未干燥即用来配制溶液;
G.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。

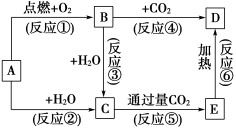
请填写下列空白:
以上反应中,属于氧化还原反应的有(填写编号)。
B→D的化学方程式:
装置B的作用是,