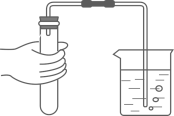
 检查装置气密性
B .
检查装置气密性
B .  向试管中加固体
C .
向试管中加固体
C .  加热液体
D .
加热液体
D . 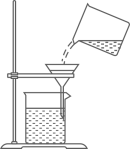 过滤
过滤

| 体液名称 | 胃液 | 血液 | 唾液 | 胆汁 |
| pH | 0.9﹣1.5 | 7.35﹣7.45 | 6.6﹣7.1 | 7.1﹣7.3 |
选项 | 宏观事实 | 微观解释 |
A | “二手烟”也会危害身体健康 | 分子在不断地运动 |
B | 氧气和液氧化学性质相同 | 同种分子性质相同 |
C | 水在直流电作用下生成氢气和氧气 | 化学变化中分子和原子种类改变 |
D | 木炭在氧气中比在空气中燃烧更剧烈 | 碳原子在等体积空间内接触碰撞的氧分子数目不同 |

加入的物质 | CuCl2溶液 | MgCl2溶液 | NH4Cl 溶液 |
实验现象 | 出现蓝色沉淀 | 出现白色沉淀 | 产生刺激性气味气体 |
选项 | 实验目的 | 实验方案 |
A | 鉴别Na2SO4、BaSO4两种白色粉末 | 加水溶解,观察现象 |
B | 除去CO中的CO2 | 将混合气体依次通过足量NaOH溶液、浓硫酸 |
C | 制备Cu(OH)2 | 向氧化铜中加入足量NaOH溶液,过滤 |
D | 比较铁和铜的金属活动性强弱 | 铁丝、铜丝分别放入稀硫酸中,观察现象 |
①一种可燃烧的金属单质;
②一种难溶于水的盐;
③用于改良酸性土壤的碱;
④导致酸雨的氧化物。
①我市是全国文明城市,作为市民更应该养成生活垃圾分类投放的良好习惯。废弃塑料瓶、书、报纸应投入印有下列哪种标识的垃圾箱。
A. B.
B. C.
C. D.
D.
②为响应“限塑令”,济南各大型超市全部更换成可降解塑料袋,其中一种可降解塑料袋的主要成分是聚乙烯醇,分子式为(C2H4O)n,聚乙烯醇属于(选填“有机物”、“无机物”、“氧化物”之一);在该物质中碳、氧两种元素的质量比为(填最简整数比),质量分数最小的元素是(填元素符号)。
③发电厂采用“石灰固硫法”来减少二氧化硫的排放,方法之一是向煤中掺入一定量的生石灰,使其与二氧化硫在高温条件下化合生成一种固体。已知这一过程中,各元素化合价均未发生变化,请写出 该“石灰固硫法”的化学方程式:。



①步骤I中若使 NaCl 不饱和溶液转变成饱和溶液,合理的方法是(填选项序号)。
A.蒸发溶剂 B.增加溶质 C.升高温度
②步骤II中用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是,NaClO 中氯元素的化合价为。
③步骤III是“侯氏制碱法”的重要步骤,写出其反应的化学方程式:。

①在t2℃时,KNO3的溶解度NaCl的溶解度(选填“大于”、“等于”或“小于”之一)。
②在t1℃时,50g 水中最多能溶解g KNO3。
③图中P点所表示的是对应温度下 KNO3的(选填“饱和”或“不饱和”之一)溶液。
④将t2℃时 KNO3饱和溶液降温到 t1℃,溶液中 KNO3 的质量分数会(选填“变大”“变小”或“不变”之一)。

①所选仪器的连接顺序为 (填写仪器序号字母)。
②生成二氧化碳时,所发生反应的化学方程式为。
③实验室制取二氧化碳后的剩余废液中常含有少量盐酸,若在不用酸碱指示剂的条件下,加入某种药品除去其中的盐酸,得到较纯净的中性液体,请从纯碱、熟石灰、石灰石三种物质中选用一种合适的试剂是,并简述实验过程。
①仪器 A 中所发生反应的化学方程式为:。
②装置B1的作用是。
③实验测得仪器 E 的玻璃管中放入的塑料试样质量为wg,塑料试样充分燃烧后,测得仪器B1质量增加ag,测得仪器B2质量增重bg,仪器C质量增重ng,则该塑料试样中含氢元素的质量为g(计算结果用代数式表示,可为分数形式)。

【信息分析】结合上述信息分析,该瓶液体一定不是溶液。
【收集证据】为了继续确定该瓶溶液的成分,小琪进行如下实验:
实验步骤 | 现象 | 结论 |
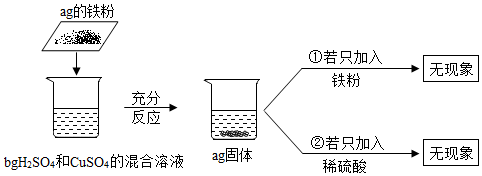
①取该溶液少量于试管中,向其中加入少许铁粉 | 无明显现象 | 该溶液不是 |
②取少量该溶液于试管中,滴加适量Ba(NO3)2 溶液,振荡 | 该溶液是 Na2SO4溶液 | |
③过滤,向滤渣中滴加过量的稀硝酸 |
根据所学知识,试写出实验步骤②中发生反应的化学方程式:。

试根据实验过程和发生的现象做出判断,填写以下空白:
①气体 G 溶于水,滴入无色酚酞试液,溶液变色。
②请写出蓝色沉淀 F 的化学式。
③混合物 B 中一定含有的物质是 (填化学式)
④无色溶液 H 中,一定大量存在的金属阳离子是 (填离子符号)。
⑤写出 1 个生成白色沉淀 I 的化学方程式。

①三星堆遗址的重大考古发现,向世界展示了中华传统文化所蕴含的丰富宝藏和巨大魅力。三星堆遗址现已出土了青铜面具、青铜神树、象牙等重要文物。青铜属于(选填“合金”“氧化物”“化合物”之一)。
②西汉刘安所著《淮南万毕术》中有关于“曾青得铁则化为铜”的记载,湿法炼铜这类化学反应属于反应。(选填“分解”“化合”“置换”“复分解”之一)
③近现代,钢铁工业的发展状况是世界各国工业化水平的重要标志之一,利用一氧化碳和氧化铁在高温条件下发生反应,是目前工业炼铁的主要原理,请你写出该反应的化学方程式:。

①当滴入稀盐酸 200g 时(即图中 B 点时),烧杯内溶液中的溶质是(填化学式)
②请读取图中信息,计算该赤铁矿石中含氧化铁的质量分数(写出计算过程,计算结果精确至 0.1%)