文物 |
|
|
|
|
选项 | A.圆雕玉舞人 | B.透雕重环玉佩 | C.朱雀青铜顶饰 | D.炫纹贯耳瓷壶 |
选项 | 劳动项目 | 化学知识 |
A | 工人用明矾处理废水 |
|
B | 工人用 |
|
C | 雕刻师用氢氟酸刻蚀石英制作艺术品 |
|
D | 酿酒师在葡萄酒中添加适量的二氧化硫 |
|
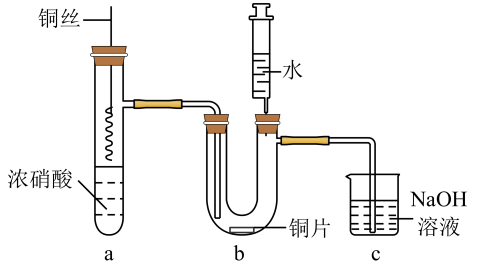

选项 | 实验 | 现象 | 结论 |
A | 向食品脱氧剂样品(含还原铁粉)中加入硫酸后滴加酸性 | 紫红色褪去 | 食品脱氧剂样品中含 |
B | 向 | 加入 |
|
C | 向 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
D | 向 | 溶液变为蓝色 | 氧化性: |

甲同学设计实验方案如下(表中溶液浓度均为):
i.实验和(填序号),探究加水稀释对水解程度的影响;
ii.实验1和3,探究加入对
水解程度的影响;
iii.实验1和4,探究温度对水解程度的影响。
序号 | 温度 | ||||
1 | 25℃ | 40.0 | 0 | 0 | |
2 | 25℃ | 4.0 | 0 | 36.0 | |
3 | 25℃ | 20.0 | 10.0 | ||
4 | 40℃ | 40.0 | 0 | 0 |
①根据甲同学的实验方案,补充数据:。
②实验测得 , 该结果不足以证明加入
促进了
的水解。根据(填一种微粒的化学式)的浓度增大可以说明加入
能促进
的水解。
③已知水解为吸热反应,甲同学预测
, 但实验结果为
。实验结果与预测不一致的原因是。
查阅资料: ,
为
溶液起始浓度。
试剂:溶液、
盐酸、
计。
实验:测定40℃下水解常数
, 完成下表中序号7的实验。
序号 | 实验 | 记录的数据 |
5 | 取 | 消耗盐酸体积为 |
6 | 测40℃纯水的 | |
7 |
在50℃和60℃下重复上述实验。
数据处理:40℃,(用含
、
、
的计算式表示)
实验结论: , 温度升高,促进
水解。
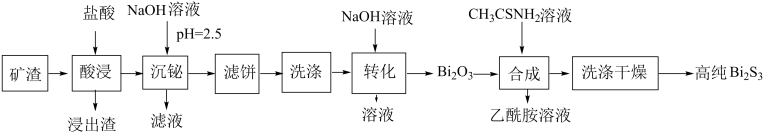
已知:
①乙酰胺()有臭味、有毒,熔点为82.3℃,沸点为221℃,可溶于水。
②常温下, ,
。
③该工艺条件下,相关金属离子形成氢氧化物沉淀的范围如下:
|
离子 |
|
|
|
|
开始沉淀的 |
1.5 |
3.6 |
4.5 |
|
沉淀完全的 |
3.2 |
4.7 |
6.7 |
回答下列问题:
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知原子1的坐标为 , 则原子2的坐标为。
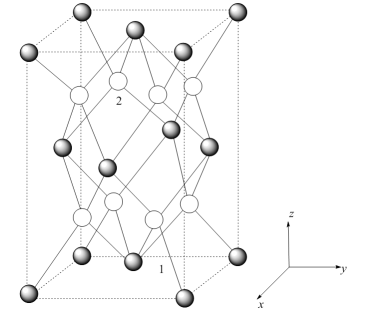
②设阿伏加德罗常数的值为 ,
的式量为
,
则晶体的密度为
(列计算式)。

①以上反应中,属于吸热反应的有(填字母)。
②平衡常数大于时可认为反应完全,则
时,反应完全进行的有(填字母)。

①图中表示的曲线为。(填“
”或“
”)。
②下列说法正确的是(填编号)。
A.当气体密度不再发生变化时,反应达到平衡状态
B.温度升高,反应的增大,
减小
C.达到平衡时分离出部分 , 反应c的平衡常数增大
D.加入稀有气体,重新达到平衡时的物质的量增加
③下达到平衡时
和
均反应完全,
、
和
的物质的量分数分别为0.20、0.32、0.12,则平衡时
的物质的量为
, 反应c的平衡常数K=。
 的分子式是。
的分子式是。
a.含有结构单元
b.含有
c.苯环上有两个取代基
 的合成路线。
的合成路线。