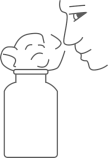
 B . 二氧化碳验满
B . 二氧化碳验满 C . 稀释浓硫酸
C . 稀释浓硫酸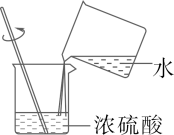 D . 检查装置气密性
D . 检查装置气密性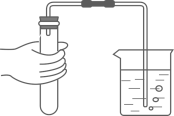

|
实验 |
A.电解水 |
B.验证硝酸铵固体溶于水吸热 |
C.区分井水和纯净水 |
D.除去河水中的泥沙 |
|
装置 |
|
|
|
|
|
分析 |
负极产生氢气 |
U型管内液面左低右高 |
观察到井水中产生大量浮渣,则X试剂为肥皂水 |
若滤液仍浑浊,可能原因是滤纸破损 |


①H2 ②2H ③2OH- ④ ⑤Fe3+
温度/℃ | 0 | 10 | 20 | 30 | 40 |
溶解度/g | 6.0 | 10.0 | 18.0 | ? | 50.0 |



A.铜、硫酸锌溶液 B.铁、硫酸铜溶液
C.铜、稀盐酸 D.铜、硫酸亚铁溶液



静置一段时间后,同学们对A中溶液的溶质成分进行探究。
猜想二:氯化钠和碳酸钠
猜想三:氯化钠和氯化钙
猜想四:氯化钠、碳酸钠和氢氧化钠
猜想五:氯化钠、氯化钙和氢氧化钠
【查阅资料】氯化钙溶液呈中性。
【实验探究】
①取样,观察溶液的颜色为红色,猜想不成立。
②然后向溶液中滴入足量稀硝酸,观察到溶液变为无色且,说明猜想二、四不成立。
③继续滴入硝酸银溶液,有白色沉淀生成,有同学据此得出猜想五成立。
【反思交流】同学们对实验③反思后认为得出的结论不严谨,理由是(用化学方程式表示)。