 B . 加热液体
B . 加热液体 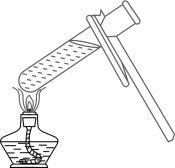 C . 收集二氧化碳
C . 收集二氧化碳 D . 闻气体气味
D . 闻气体气味





温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |



①应选择的发生装置是;
②反应的化学方程式为;
③当观察到现象时,证明气体已收集满。
A.“可燃冰”就是冰
B.“可燃冰”有可能成为人类未来的重要能源
C.“可燃冰”的实质是水变成的石油
【查阅资料】Ⅰ、草酸钙是一种白色晶体,不溶于水,高温灼烧时可能生成成 CaCO3或 CaO;
Ⅱ、NaOH 溶液可吸收 CO2 , 但不能吸收 CO。
【进行实验】称取一定量的草酸钙,按照下图装置进行实验。

【分析讨论】
经称量,装置 B 增重 2.2g,试求 B 装置中参加反应的 NaOH 的质量。
解:设参加反应的 NaOH 的质量为 x。
列比例式:
求解:x=
答:略。
【猜想假设】猜想 1:CaCO3 猜想 2:CaO 猜想 3:
【进行实验】向反应后固体中加入足量水,温度升高,此反应的化学方程式为,再向其中加入足量稀盐酸,无明显现象。
【得出结论】Ⅰ、根据现象,猜想正确;
Ⅱ、结合实验现象,写出 CaC2O4分解的总反应化学方程式为。