 称量食盐
B .
称量食盐
B .  向试管中加锌粒
C .
向试管中加锌粒
C .  鉴别氯化钾和氯化铵
D .
鉴别氯化钾和氯化铵
D . 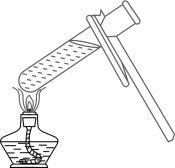 加热液体
加热液体


①NaOH固体和水 ②硝酸铵固体和水 ③锌和稀硫酸 ④碳酸钠粉末和稀盐酸 ⑤生石灰和水 ⑥二氧化锰和过氧化氢溶液
选项 | 实验目的 | 实验方案 |
A | 分离KCl、MnO2固体混合物 | 溶解,过滤 |
B | 鉴别氯化钠和硝酸铵固体 | 加水溶解 |
C | 检验氯化钙溶液中是否混有盐酸 | 取样,滴加酚酞溶液 |
D | 除去铜粉中的碳粉 | 在空气中充分灼烧 |



 图1,电解水
B .
图1,电解水
B .  图2,加热碳和氧化铜的混合物
C .
图2,加热碳和氧化铜的混合物
C .  图3,用等质量、等浓度的双氧水分别制取氧气
D .
图3,用等质量、等浓度的双氧水分别制取氧气
D .  图4,向一定质量的稀盐酸中逐滴加入氢氧化钙溶液
图4,向一定质量的稀盐酸中逐滴加入氢氧化钙溶液
①下列物品中,由有机合成材料制成的是(填字母)。
a. 塑料油桶 b.
塑料油桶 b. 纯棉帽子 c.
纯棉帽子 c. 碳纳米管
碳纳米管
②C919飞机机身蒙皮使用了铝锂合金材料。下列不属于铝锂合金性质的是(填字母)。
a.密度大 b.硬度高 c.抗腐蚀


a.甲试管中固体增多 b.乙试管中固体减少
c.甲试管中溶液的溶质质量分数不变 d.乙试管中溶液仍饱和


[提出问题]固体样品的成分是什么?
[查阅资料]
①碱石灰干燥剂是CaO和NaOH的混合物。
②BaCl2溶液显中性。
[猜想与假设]
固体样品中可能含有Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和等七种物质。
[进行实验]
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①滤渣完全溶解,溶液变为黄色② | 结论:滤渣B中有Fe2O3、CaCO3.实验操作中Fe2O3与稀盐酸反应的化学方程式为 |
乙组同学对滤液C的成分进行了探究。记录如下:
实验操作 | 实验现象 | 实验结论 |
取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成②酚酞试液由无色变成红色 | 滤液C中有 |
[解释与结论]乙组同学实验中加入过量BaCl2溶液的目的是。

①制取NO2的发生装置可选用,写出反应的化学方程式。
②若用D装置来收集NO2气体应从接口(填标号)处进入集气瓶。从环保的角度考虑,在制取NO2时若在装置D后连接的装置是E,你认为要将E中的浓硫酸换成(填具体的溶液)。
a.装置A和装置B的气密性检查的操作方法相同
b.装置B发生反应时,仪器②下端需要浸没在液体中
c.E装置可用于干燥气体,气流方向为c进d出
d.若挤压F中试管上方的滴管,可以观察到U型管左边液面上升
