目的 | 操作 | |
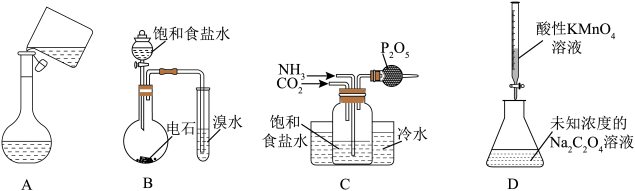
A | 验证淀粉未水解 | 向淀粉溶液中加适量20%H2SO4溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,观察颜色变化。 |
B | 验证 | 室温下,用pH试纸测得:0.1mol/LNa2SO3溶液的pH约为10;0.1mol/LNaHSO3溶液的pH约为5. |
C | 探究维生素C的还原性 | 向盛有2mL黄色FeCl3溶液的试管中滴加浓的维生素C溶液,观察颜色变化。 |
D | 研究温度对化学平衡的影响 | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温,观察颜色变化。 |
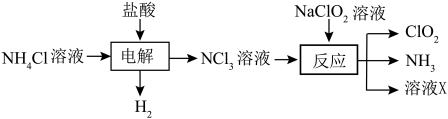
已知:①电解过程中氯元素被氧化。
②ClO2是一种黄绿色易溶于水的气体;三氯化氮为黄色油状液体,熔点较低,很不稳定,受热90℃以上或受震动时发生猛烈爆炸。下列说法正确的是
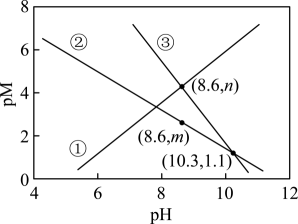
[已知:;
, M为
或
]下列说法正确的是
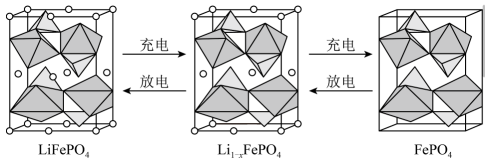
下列说法正确的是
①![]() 和
和![]() 中所有原子均共面,其中氮原子较易形成配位键的是。
中所有原子均共面,其中氮原子较易形成配位键的是。
②配位原子提供孤电子对的能力与元素的电负性大小有关,元素电负性越大,其原子越不容易提供孤电子对。则对于配合物Fe(SCN)3 , 配体SCN-中提供孤电子对的原子是(填元素符号)。
③将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是。
A.[Cu(NH3)2]Cl B.[Cu(NH3)4]SO4
C.[Zn(NH3)4]SO4 D.[Cr(H2O)5Cl]Cl2
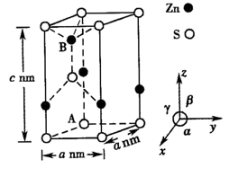
①该晶体中,锌的配位数为。
②已知空间利用率 , 设锌和硫的原子半径分别r1cm和r2cm,则该晶体的空间利用率为(列出计算式即可)。
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。若A点原子的分数坐标为(0,0,0),则B点原子的分数坐标为。
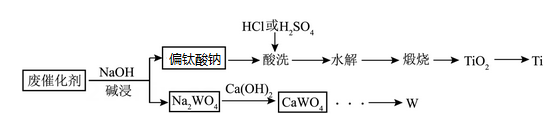
已知:①偏钛酸钠(Na2TiO3)难溶于水;“酸洗”时,Na2TiO3转化为TiOCl2或TiOSO4 , 水解后得到H2TiO3;
②当溶液中某离子浓度≤1×10-5mol/L时,认为该离子沉淀完全。
请回答下列问题:


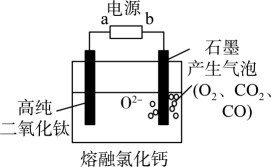
已知:①氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇;
②VO2+有较强还原性,易被氧化。
实验室以V2O5为原料制备该晶体的流程如图:
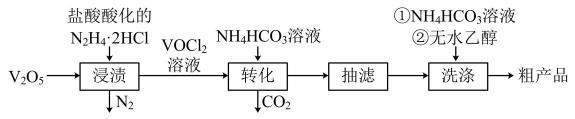
请回答下列问题:

①上述装置连接的合理顺序为e→(按气流方向,用小写字母表示)。
②写出装置D中生成氧钮(Ⅳ)碱式碳酸铵晶体的化学方程式。

①滴定终点时的现象为。
②粗产品中钒元素的质量分数为%。
①仅含-CHO、-OH、-C3H7和苯环结构;
②核磁共振氢谱峰面积之比为1:1:2:2:6.
 的合成路线。
的合成路线。
①
H
②
H1=+40.9kJ/mol
③
H2=-90.4kJ/mol
试计算HkJ/mol。

①投料比n(CO2):n(H2)=l:3的曲线是。(填“a”、“b”或“c”)
②已知点N在曲线b上,计算该温度下压强平衡常数Kp=(MPa)-2.(用平衡分压代替平衡浓度计算)
③该温度下,测得某时刻p(CO2)=0.2MPa,p(CH3OH)=p(H2O)=0.1MPa,p(H2)=0.4MPa,此时v正:v逆=。(保留2位有效数字)

①该反应的活化能Ea=kJ/mol。
②当用更高效催化剂时,请在图中画出Rlnk与关系的曲线。

①温度为T1时,该反应的正反应速率v(B)正v(A)逆(填“>”,“=”或“<”)。
②B、C、D三点逆反应速率由大到小的顺序为。[用“v(D)”、“v(C)”、“v(B)”表示]