A | B | C | D |
|
|
|
|
工业合成乙烯 | 生产橡胶 | 侯氏制碱 | 人工合成结晶牛胰岛素 |
A | B | C | D |
|
|
|
|
复原变形金属 | 补配玉器缺损 | 青铜器除锈见新 | 剥离丝绸残片 |
 D .
D . 选项 | 劳动项目 | 化学知识 |
A | 明矾净水 | 明矾具有氧化性 |
B | 小苏打用作发泡剂烘焙面包 | 小苏打受热分解产生气体 |
C | 用热的纯碱溶液洗去油污 | 热的纯碱溶液水解显碱性 |
D | 用厨余垃圾制肥料 | 厨余垃圾含N、P等元素 |
X | Y | |
Z | W |
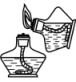 B . 称量10.05g固体
B . 称量10.05g固体 C . 检查容量瓶是否漏水
C . 检查容量瓶是否漏水 D . 稀释浓硫酸
D . 稀释浓硫酸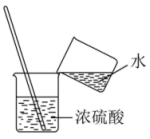
甲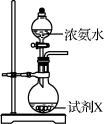 乙
乙 丙
丙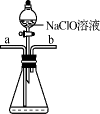 丁
丁
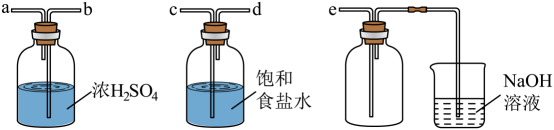
①下列操作步骤的正确顺序为(填字母)。
a.体系冷却后,停止通入 b.通入干燥的
赶尽装置中的空气
c.在铁屑下方加热至反应完成 d.用干燥的赶尽
e.检验装置的气密性
②该实验装置存在的明显缺陷是。
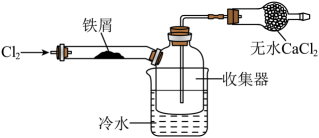
已知: ,
。
有关物质的熔、沸点如下表:
物质 | 熔点/℃ | 沸点/℃ |
-59 | 11 | |
-107 | -34.6 |
的生产流程示意图如下:

该工艺中,需要补充的物质X为(填化学式,下同),能参与循环的物质是。从发生器中分离出
, 可采用的方法是。
②“酸浸”时,发生反应的离子方程式是。
步骤一:取溶液,将其稀释成100.00mL溶液。
步骤二:取25.00mL稀释后的溶液,向其中加入酸性
溶液。恰好反应时,记下消耗
溶液的体积。
步骤三:重复上述实验3次,平均消耗溶液20.00mL。
已知:(未配平)
①配平上述方程式。
②“步骤一”中稀释时所用的水需先进行加热煮沸,其目的是。
③试通过计算,求原溶液的物质的量浓度是多少?(写出计算过程)
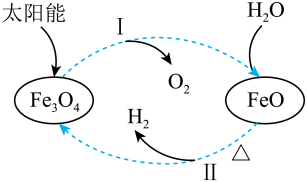
在催化剂的作用下,氢气还原的过程中可同时发生反应①②。
①
②
总压/ | ||||||
起始 | 0.5 | 0.9 | 0 | 0 | 0 | |
平衡 | m | 0.3 | p |
已知 , 则表中
;反应①的平衡常数
(用含p的代数式表示),
为压强平衡常数,是在化学平衡体系中,用各气体物质的分压替代浓度计算的平衡常数。
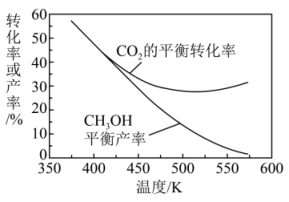
图中500K以后,的平衡转化率随温度升高而增大的原因是。
①遇氯化铁溶液能发生显色反应;②能与NaHCO3反应产生气体。
其中核磁共振氢谱上有5组峰且峰的面积比为1∶2∶2∶2∶1的结构简式为。