
①恰好完全反应时,一定没有固体剩余
②x的值为0.2
③铁样品中可能含有镁
④M点对应的溶液中含有2种或3种溶质


| 物质名称 | 西红柿汁 | 柠檬汁 | 牛奶 | 小苏打水 |
| pH范围 | 4~5 | 2~3 | 6~7 | 8~9 |
 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 测溶液的pH
C . 测溶液的pH  D . 除去H2中的HCl
D . 除去H2中的HCl 


①图中a点的含义是,60℃时,两物质中溶解度较大的是;
②当硝酸钾中含有少量氯化钠时,可采用的方法提纯硝酸钾;
③将氯化钠的饱和溶液转化为同温下的不饱和溶液,可采用的方法是;
④如图所示,10℃时向硝酸钾溶液(底部有Xg硝酸钾晶体)中加入10g水并充分搅拌,恢复至10℃,正确的说法是。

A.所得溶液一定饱和
B.溶质质量一定变大
C.溶质质量分数可能变大
D.若X< 2.1g,所得溶液不饱和
⑤工业上用电解饱和食盐水的方法制取氢氧化钠。反应原理是:
2NaCl+2H2OH2↑+Cl2↑+2NaOH。
Ⅰ.该实验中正极产生的气体呈黄绿色,具有刺激性气味,该气体是(填“H2”或“Cl2”)。向电解后的溶液中滴加硫酸铜溶液,可观察到,证明反应生成了氢氧化钠。
Ⅱ.电解食盐水时,若有0.5molNaCl参加反应,生成氢氧化钠的质量是g。(根据化学方程式列式计算)


a.生石灰 b.硝酸铵 c.氯化钠 d.氢氧化钠固体
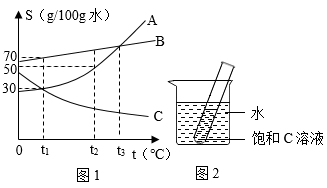
①t1℃时,将C物质的不饱和溶液变为饱和溶液,溶质的质量分数一定变大
②t2℃时,取等质量的A、B两种物质的饱和溶液分别蒸发等量的水后,恢复到t2℃,析出晶体的质量A<B
③t3℃时,A、B、C三种物质溶解度的大小关系是A=B>C