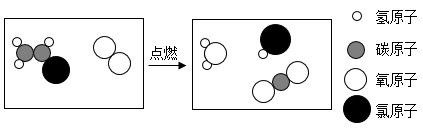
 B . 世界之窗的焰火表演
B . 世界之窗的焰火表演 C . 大梅沙海滩的沙
C . 大梅沙海滩的沙 D . 深圳欢乐谷的漂流
D . 深圳欢乐谷的漂流
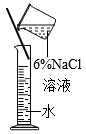 B . 镁条的燃烧
B . 镁条的燃烧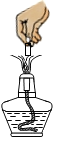 C . 氯酸钾加热分解
C . 氯酸钾加热分解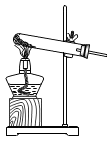 D . 验证分子运动
D . 验证分子运动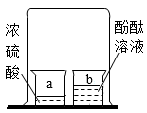

选项 | 物质(括号内为杂质) | 验目的 | 方法 |
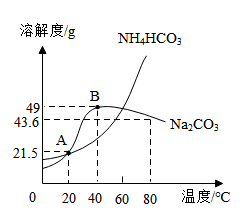
A | NH4NO3固体与NaOH固体 | 鉴别 | 加水,溶解 |
B | 软水与硬水 | 鉴别 | 加肥皂水振荡,观察 |
C | NaCl (Na2CO3) | 除杂 | 加入足量的稀盐酸,蒸发 |
D | CO2(CO) | 除杂 | 通过盛有NaOH溶液的洗气瓶 |
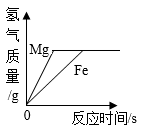 图像①表示向等质量、等质量分数的稀硫酸中分别加入过量的镁粉和铁粉
B .
图像①表示向等质量、等质量分数的稀硫酸中分别加入过量的镁粉和铁粉
B . 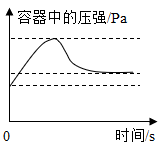 图像②表示在密闭容器中用红磷来测定空气中氧气含量时的压强变化
C .
图像②表示在密闭容器中用红磷来测定空气中氧气含量时的压强变化
C . 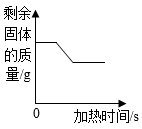 图象③表示加热时CO还原CuO过程中剩余固体的质量变化
D .
图象③表示加热时CO还原CuO过程中剩余固体的质量变化
D . 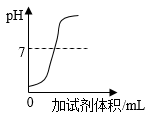 图像④表示向稀盐酸中滴加氢氧化钠溶液时pH值的变化
图像④表示向稀盐酸中滴加氢氧化钠溶液时pH值的变化


【查阅资料】①无水硫酸铜是白色粉末,易吸水变蓝,遇HCl无明显现象
【猜想假设】猜想一:该气体为H2、H2O;
猜想二:该气体为H2、HCl;猜想三:该气体为。
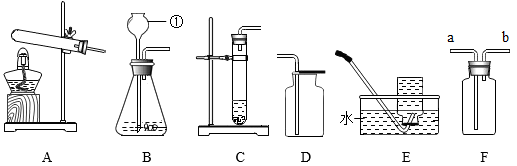
小力同学查阅资料后,设计了下列实验验证猜想:
实验Ⅰ | 实验Ⅱ | |
操作 |
|
|
现象 | A中白色无水硫酸铜变为色,B中固体由黑色变成红色 | D中产生色沉淀,且沉淀不溶于稀硝酸 |
结论 | 猜想成立 | |
小力同学利用锌粒与稀盐酸制得的H2中含有猜想三的杂质气体,他决定利用图示实验装置除去混有的气体,G瓶中发生反应的化学方程式为。

综合考虑利弊后,实验室制取氢气常用稀硫酸而不用稀盐酸。
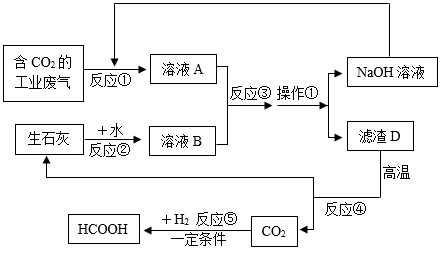
根据以上流程图回答下列问题:
时间/min | t1 | t2 | t3 | t4 | t5 |
杯中物质总质量/g | 119 | 118 | 117 | 116 | 116 |
①由题所述,LiH在实验室保存时应注意保持;
②在t4时间节点,LiH恰好完全反应,反应产生的氢气总质量为g;
③求样品中氢化锂的质量分数。