
查阅资料可知洁厕灵(如图)的有效成分是HCl。HCl的含量可利用NaHCO3溶液来测定,反应的化学方程式为HCl+NaHCO3=NaCl+H2O+CO2↑,洁厕灵其他成分均不参加反应。向一锥形瓶中加入100克该品牌洁厕灵,再逐次加入相同质量分数的NaHCO3溶液,测出每次锥形瓶中充分反应后溶液的总质量,数据记录如表。

|
第一次 |
第二次 |
第三次 |
|
|
加入NaHCO3溶液的质量/克 |
100 |
100 |
100 |
|
反应后溶液的总质量/克 |
197.8 |
295.6 |
395.6 |
| 装置 | A | B |
| 注射器内试剂 | 10mL ▲ | 10mL20%的盐酸 |
| U形管内试剂 | 10mL饱和碳酸钠溶液 | 10mL饱和碳酸钠溶液 |
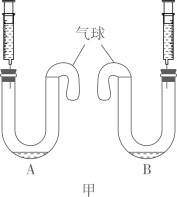
装置A中注射器盛放的试剂为。
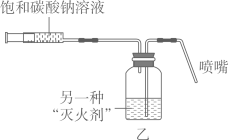
小金制作了如图乙所示灭火器,推动注射器活塞,喷嘴喷出液体将燃烧的蜡烛熄灭,蜡烛熄灭的原因是。

| 实验 | 氧气含量 | 二氧化碳含量 | 蜡烛能否燃烧 |
| A | 21% | 8.4% | 能 |
| B | 21% | 3.4% | 能 |
| c | 12.8% | 3.4% | 不能 |
[建立假设]H2O2溶液浓度越小,产生氧气的速度越慢,
[实验方案]在相同条件下,分别用30毫开2%、4%和6%的H2O2溶液进行实验,记录收集20毫升氧气所需的时间。

[实验数据]
实验序号 | 1 | 2 | 3 |
H2O2溶液的浓度 | 2% | 4% | 6% |
收集20毫升氧气所需时间/秒 | t1 | t2 | t3 |
[实验结论]在相同条件下,H2O2溶液浓度越小,产生氧气的速度越慢。