
选项 | 被提纯的物质 | 除杂试剂及分离方法 |
A | | 过量的澄清石灰水,过滤 |
B | Fe2O3(SiO2) | 加入HCl溶液后过滤,洗涤 |
C | 乙烷(乙烯) | 将混合气体通入盛有酸性 |
D | 乙醇(水) | 加入适量生石灰后,蒸馏 |

①金属铝与氢氧化钠溶液反应
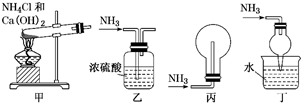
②NH4Cl固体与Ca(OH)2固体制备NH3
③Na在Cl2中燃烧
④水蒸气变成液态水
⑤硫酸和氢氧化钡溶液反应
⑥碳酸氢钠热分解

 和
和 C .
C . 
选项 | 实验操作和现象 | 实验结论 |
A | 相同条件下,将同等大小的钠分别加入无水乙醇和水中,钠与水反应更剧烈 | 乙醇中氢的活泼性比水中氢的活泼性弱 |
B | 向淀粉溶液中加入适量稀硫酸,加热,冷却后加入过量NaOH溶液至碱性,再加少量碘水,溶液不变蓝 | 淀粉完全水解 |
C | 向2mL 0.01 | 该反应存在限度 |
D | 在烧杯中将氢氧化钡晶体和氯化铵晶体混合搅拌,片刻后用手触摸烧杯底部感到冰凉,同时有刺激性气味的气体生成 | 该反应为放热反应 |


足量B通入溴水中的现象是;体现了B的性。
t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.012 | 0.008 | 0.005 | 0.004 | 0.004 |
①0~4s内,。
②在第5s时,的转化率为。
③由数据推测,反应在第4s时恰好达到平衡状态。该推测(填“正确”或“错误”)。

①氢氧燃料电池的在导线中电子的方向为由(用a、b表示)。
②溶液中OH- 移向电极(填“A”或“B”)。
③该原电池的B极发生(填“氧化”或“还原”)反应,该电极的反应式为。

步骤①中获得Br2的离子方程式为;步骤③的化学方程式为;目的为 。

① 设计“操作Ⅰ”的主要步骤:溶解、。
② “试剂a”通常应具有一定的性。
③ 利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
KI+H2O2=KOH+I2
④ 由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是。(选填编号)
试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
⑤“操作II”宜选用的装置是。(选填编号)
A.![]() B.
B.![]() C.
C. D.
D.![]()
⑥在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:。