 点燃镁条
B .
点燃镁条
B . 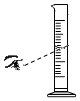 读取液体体积
C .
读取液体体积
C . 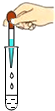 滴加液体
D .
滴加液体
D . 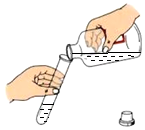 倾倒液体
倾倒液体
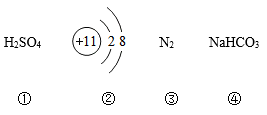
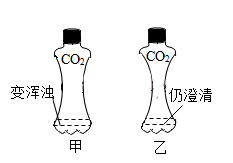
选项 | A | B | C | D |
实验 方案 |
|
|
|
|
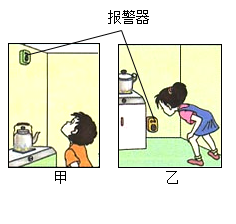
现象 | 铁丝在空气中只发生红热;在氧气中剧烈燃烧,火星四射,生成黑色固体 | ①中白磷不燃烧,②中红磷燃烧 | 干燥石蕊试纸不变色,湿润石蕊试纸变红 | 蜡烛由高到低依次熄灭 |
结论 | 氧气浓度越大,燃烧越剧烈 | 可燃物燃烧的条件之一是温度达到着火点 | HCl气体溶于水后溶液的pH>7 | CO2密度比空气大,不燃烧也不支持燃烧 |
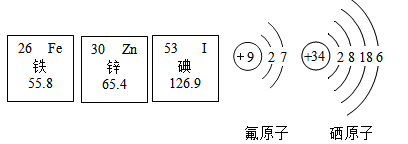
温度/℃ | 20 | 30 | 40 | 60 | 80 | 100 | |
溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | 39.8 |
KNO3 | 31.6 | 45.8 | 63.9 | 110 | 169 | 246 | |

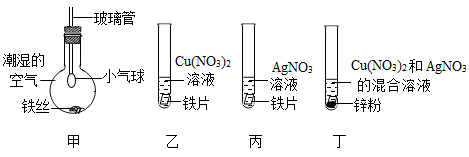
方案一:取少量溶液B
方案二:取少量溶液B
①写出方案二中产生沉淀的化学反应方程式。
②方案(填“一”或“二”)合理。

【查阅资料】
物质 | Na2CO3 | Na2SO4 |
溶解度/g(20℃) | 21.8 | 19.5 |
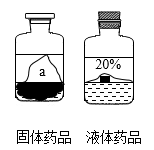
步骤一:取样品少许于试管中,加入一定量的水,手握试管,感受到试管发烫。小明判断:该试剂为NaOH固体。同学们认为小明的判断不准确,因为。
步骤二:取步骤一所得上层清液,加入少量Na2CO3溶液,看到产生白色沉淀。得出准确结论:该固体药品是。写出生成沉淀的化学反应方程式:。
步骤三:通过查阅资料,小组同学讨论分析,该瓶液体药品不可能是Na2CO3溶液和Na2SO4溶液,原因是。
步骤四:小组同学设计如下实验对液体药品进行探究。
实验操作 | 实验现象 | 实验结论 |
①取少量待测液于试管中,滴加过量的Ba(NO3)2溶液 | 有白色沉淀 | 该液体试剂中含Na2CO3、Na2SO4、NaCl,该瓶NaCl溶液被污染 |
②在①反应后的试管中滴加过量的 | ||
③将②反应液静置,继续滴加适量的AgNO3溶液 | 有白色沉淀 |
a.NH4H2PO4
b.KCl
c.CO(NH2)2