选项 | 探究方案 | 探究目的 |
A | 用毛皮摩擦过的带电橡胶靠近 |
|
B | 将铁锈溶于浓盐酸,滴入 | 铁锈中含有二价铁 |
C | 石蜡油加强热,将产生的气体通入溴水,溴水颜色褪去 | 气体中含有乙烯 |
D | 用pH计分别测0.1 |
实验 | 实验操作与现象 |
1 | 测得0.1 |
2 | 向5mL 0.1 |
3 | 将沉淀X加入5mL 2 |
4 | 将沉淀Y溶于足量2 |
已知: ,
。下列说法正确的是( )
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
平衡时和CO的选择性、乙醇的转化率随温度的变化曲线如图所示。

已知:CO的选择性=。
下列说法正确的是( )
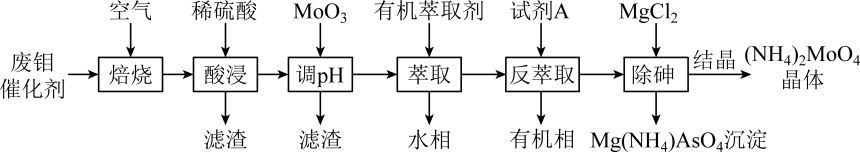
注:酸浸后钼元素以MoO形式存在。
回答下列问题:
已知:溶液中某离子浓度≤10-5mol•L-1时,认为沉淀完全;常温下Ksp[Fe(OH)3]=10-38.5 , Ksp[Cu(OH)2]=10-19.6。
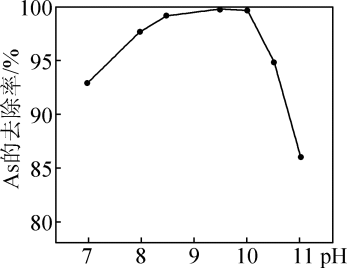
已知:(NH4)3H4PMo12O42•H2O+26NaOH=12Na2MoO4+Na2HPO4+3NH3↑+17H2O。
①苯环上有三个取代基,苯环上的一氯代物有两种,且分子中有5种不同化学环境的氢原子;
②能发生水解反应,且水解产物之一能与溶液发生显色反应;
③能发生银镜反应。
Ⅰ.制备硫代硫酸钠
反应原理:。实验装置如图所示。
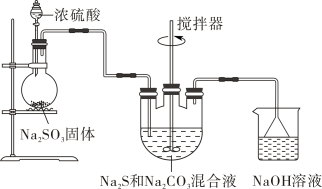
在和
的混合溶中不断通入
气体,三颈烧瓶中的现象为:
①浅黄色沉淀逐渐增多。原理为:
②浅黄色沉淀保持一段时间不变,有无色无味气体产生。原理为:
③浅黄色沉淀逐渐减少。
④继续通入 , 浅黄色沉淀又逐渐增多。原理为:
经预处理的芯片中含有游离态的Au,用单一的溶液处理,金的浸取率极低。
向浸取液中通入空气使Au转化为稳定性高的
, 该反应的离子方程式为。


①向银氨溶液中加入溶液,离心分离、洗涤干燥后可得到
高效光催化剂,写出反应的离子方程式为。
②和
在溶液中反应也可制得
固体,但制得的
固体光催化性能极差。从速率角度解释其原因是。
