 取用大理石
B .
取用大理石
B .  点燃酒精灯
C .
点燃酒精灯
C . 
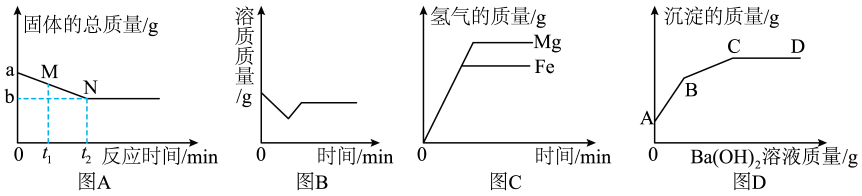
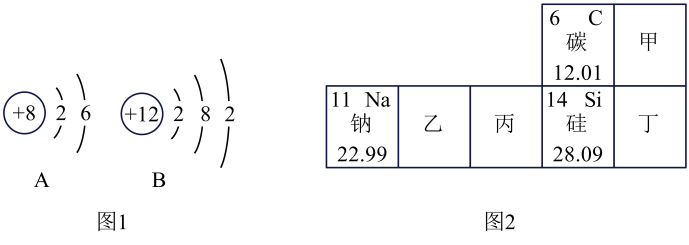
①A原子的质子数是。钠元素的相对原子质量是,B所示原子对应元素在元素周期表中的位置是(填“甲”“乙”“丙”或“丁”)。
②芯片主要由硅材料制成。硅属于(填“金属”或“非金属”)元素,图2中与硅元素属于同一族的元素是。
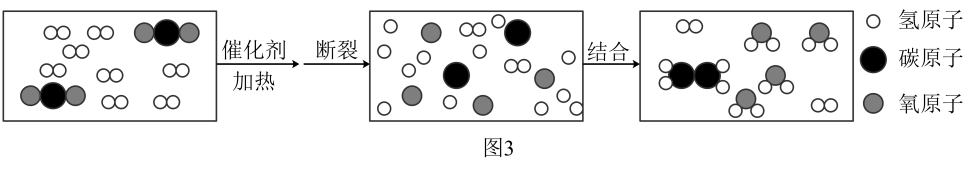
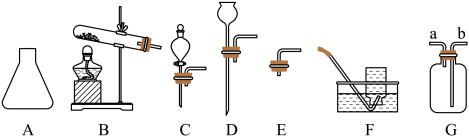
方案一:重新组合发生装置,需选择图中的装置有(填字母)。
方案二:20℃时,把上述盐酸稀释为质量分数为5%的盐酸,下列不需要用到的仪器有(填序号)。此时取用15%的盐酸与水的质量比为。
①烧杯②量筒③药匙④胶头滴管⑤玻璃棒⑥酒精灯
①收集氧气、二氧化碳;②G中盛氢氧化钠溶液,除去二氧化碳中的氯化氢气体;③G中盛浓硫酸,除去氧气中的水蒸气;④G中盛紫色石蕊溶液,检验二氧化碳;⑤G中盛满水,b口连接量筒,测量生成的二氧化碳体积。
①请写出一种爱护水资源措施,一种净化水的方法。
②水是化学学习中的重要物质,水在化学学习中的用途是。(一条即可)
温度(℃) | 0 | 20 | 40 | 60 | 80 |
溶解度(g) | 33 | 46.5 | 65.5 | 139 | 153 |
①醋酸钠溶液在太空中形成液体球,用带有结晶核的绳子接触液体球,它就会瞬间变成“冰球”。该过程属于(选填“结晶”或“溶解”)。
②完成上述实验需配制溶质质量分数为60%的100g醋酸钠溶液,其主要操作是。
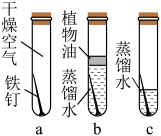
步骤 | 现象 | 化学方程式 |
向C试管中再加入(填一种即可)溶液,产生白色沉淀,证明NaOH溶液与CO2能发生化学反应。
将氢氧化钠溶液与盐酸混合,进行如图2所示实验。试管中溶液的pH随滴加溶液体积的变化曲线如图3所示。则溶液Y中溶质是,反应的化学方程式为。滴入的溶液体积为VmL时,点M处的混合溶液中所含微观粒子有。
由以上实验,可归纳氢氧化钠的化学性质有。